2. 农业部海洋渔业可持续发展重点实验室中国水产科学研究院黄海水产研究所 青岛 266071;
3. 青岛海洋科学与技术国家实验室海洋渔业科学与食物产出过程功能实验室 青岛 266071
2. Key Laboratory of Sustainable Development of Marine Fisheries, Ministry of Agriculture, Chinese Academy of Fishery Sciences, Yellow Sea Fisheries Research Institute, Qingdao 266071 ;
3. Laboratory for Marine Fisheries Science and Food Production Processes, Qingdao National Laboratory for Marine Science and Technology, Qingdao 266071
三疣梭子蟹(Portunus trituberculatus)隶属甲壳纲(Crustacea)、十足目(Decapoda)、梭子蟹科(Portunidae)、梭子蟹属(Portunus),广泛分布于中国近海、日本、朝鲜半岛及马来西亚群岛等海域,是我国重要的海产经济蟹类,也是海水人工养殖的主要种类之一(戴爱云等, 1977、1986),具有产量大、营养价值高等优点,1981年以来已被列为我国海洋水产养殖对象(孙颖民等, 2005)。盐度是三疣梭子蟹养殖中重要的环境因素之一,对其呼吸、代谢、生长、存活以及免疫防御有着极其重要的影响(周双林等, 2001)。
甲壳类渗透压调节机理研究主要集中于离子转运机制,其中主要依靠Na+-K+-ATPase调节细胞内Na+、K+含量的稳定(江山等, 2011)。游离氨基酸(FAAs)在甲壳动物渗透压调节中也具有重要作用(Clark, 1968; Boone et al, 1977; Dalla-Via, 1986)。Dalla-Via (1986)发现,甘氨酸(Gly)、脯氨酸(Pro)、精氨酸(Arg)、丝氨酸(Ser)、苏氨酸(Thr)及丙氨酸(Ala)是凡纳滨对虾(Lieopenaeus vanamei)渗透压调节的主要贡献者。Fang等(1992)研究发现,当外界盐度发生变化时,Gly、Pro、Ala、Arg、Tau在调节斑节对虾(Penaeus monodon)体内渗透压方面具有主要作用。本课题组通过比较转录组学研究发现,不同盐度胁迫下,差异表达基因也富集于一些FAAs通路(Lv et al, 2013)。然而,目前尚未见蟹类相关研究报道,其体内的FAAs是否在渗透压调节中发挥相似或有别于对虾类的功能值得进一步研究。
1 材料与方法 1.1 实验材料实验于2015年7月在中国水产科学研究院黄海水产研究所昌邑市海丰水产养殖有限公司实验基地进行,取健康三疣梭子蟹,个体平均体重为(100±10.0) g,暂养于3 m3的室内水池中,水温为(25.0±3.0)℃,盐度为33,持续充氧,每天更换1/3体积的海水,定时喂食蓝蛤。
1.2 实验方法实验盐度分别为10、20、40和50,每组3个重复,对照组为海水(盐度为33),盐度胁迫5 d后,随机从每个实验组中抽取10只蟹,取其鳃组织约1.5 g左右,加入5 ml 8%的三氯乙酸(TCA),沉淀蛋白,超声波破碎,使之均质,1℃、13000 r/min离心20 min,保留上清液,用TCA再提取2次,收集上清液,加乙醚30 ml,振荡30 s,水层用低压旋转蒸发器浓缩至近干,浓缩物用0.02 mol/L盐酸定容至10 ml,以日立835-50型氨基酸自动分析仪进行FAAs测定(Dalla-Via, 1986; Shewbart et al, 1972; McCoid et al, 1984)。
1.3 数据的统计学分析采用STATISTIC软件对数据进行统计学分析。先对数据作方差分析,若有显著差异,再作Duncan’s多重比较。结果用“平均数±标准差”表示,P < 0.05为差异显著。
2 结果 2.1 正常海水鳃组织中游离氨基酸的组成与含量实验共检测了18种FAAs,总含量为6.34 mg/g,其中Tau含量最高(2.54 mg/g),占总量的40.06%,其次分别为Ala (0.65 mg/g)、Glu (0.64 mg/g)、Arg (0.58 mg/g)、Gly (0.48 mg/g)和Pro (0.25 mg/g),含量最低的为甲硫氨酸(Met, 0.02 mg/g),分别占总游离氨基酸(TOFAA)的10.25%、10.09%、9.15%、7.57%、3.94%和0.32% (表 1)。所检测FAAs中包含9种必需氨基酸(EAA) (Thr、Val、Met、Ile、Leu、Phe、Lys、His和Arg)和9种非必需氨基酸(NEAA) (Glu、Ala、Gly、Asp、Ser、Cys、Tyr、Pro和Tau),分别占TOFAA含量的20.88%和79.12%。其中,NEAA中的Asp、Glu、Gly和Ala属鲜味氨基酸(TAA),分别占TOFAA和NEAA含量的29.07%和36.74%。(Glu、Ala、Gly、Asp、Ser、Cys、Tyr、Pro和Tau),分别占TOFAA含量的20.88%和79.12%。其中,NEAA中的Asp、Glu、Gly和Ala属鲜味氨基酸(TAA),分别占TOFAA和NEAA含量的29.07%和36.74%。
|
|
表 1 不同盐度下三疣梭子蟹鳃中游离氨基酸的含量 Table 1 Concentrations of free amino acids in the gills of P. trituberculatus under different salinities (mg/g, mean±SD) |
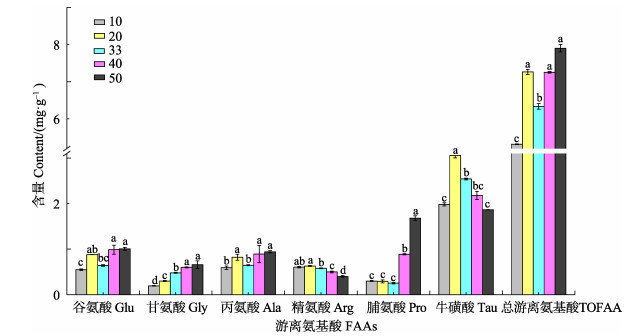
随盐度改变,鳃中大多数FAAs含量发生显著变化,总体趋势为FAAs含量随着外界盐度的升高而升高(P < 0.05),盐度50时,TOFAA为盐度10时的1.48倍。Gly、Glu、Ala和Pro的含量与盐度呈现显著正相关,其中,浓度变化最大的为Pro,盐度50时,其浓度为盐度10时的5.60倍,其次为Gly(3.47倍)、Glu(1.84倍)、Ala(1.59倍)。另外发现,Arg含量与盐度呈显著负相关,盐度50时的浓度为盐度10时浓度的0.67倍。含量较高的Tau与其他FAAs随着盐度的升高无显著变化(图 1、表 1)。
|
图 1 盐度胁迫下三疣梭子蟹鳃组织中游离氨基酸的变化情况 Figure 1 Variations in the concentrations of free amino acids in the gills of P. trituberculatus under different salinities |
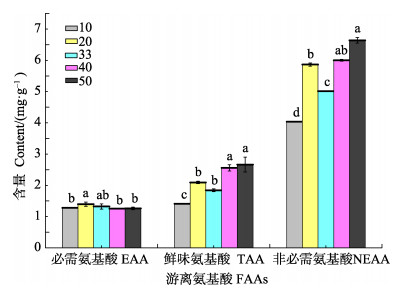
实验分析了EAA和NEAA在盐度胁迫下的浓度变化趋势,结果显示,鳃组织中EAA的总量随盐度的变化并无显著性的改变,而NEAA的总量随外界盐度的升高而显著增加,盐度50时NEAA的含量为盐度10时的1.64倍。另外,TAA的浓度也与外界盐度呈显著正相关(P < 0.05)(图 2)。
|
图 2 三疣梭子蟹鳃组织中必需氨基酸和非必需氨基酸对盐度胁迫的响应 Figure 2 Concentrations of essential amino acids and non-essential amino acids in the gills of P. trituberculatus in response to different salinities |
鳃是甲壳动物渗透压调节的重要场所与器官(潘鲁青等, 2005),本研究通过检测和分析不同盐度环境下三疣梭子蟹鳃组织中FAAs的含量及浓度变化规律,明确FAAs的组成及在盐度适应中发挥的功能,丰富FAAs在甲壳动物盐度适应中的重要作用,为深入研究其分子机理提供数据支持。
研究发现,Tau在正常海水三疣梭子蟹鳃中含量最高,其次为Ala、Glu、Arg、Gly、Pro。该结果与Gerard等(1972)研究蓝蟹(Callinectes sapidus)中得到的结果一致,而相比对虾存在一定的差别。梁萌青等(2009)、黄凯等(2010)研究发现,凡纳滨对虾血淋巴和肌肉中含量最高的FAAs为Gly,可能是因为物种的差异性或分析的组织不同所造成的。当盐度升高时,三疣梭子蟹鳃中的TOFAA的含量显著增加(P < 0.05),盐度50时TOFAA为盐度10时的1.48倍,上升幅度最大的FAAs依次为Pro (5.60倍)、Gly (3.47倍)、Glu (1.84倍)和Ala (1.59倍),表明其在三疣梭子蟹盐度适应中发挥渗透压调节功能。该结果与McCoid等(1984)与Fang等(1992)认为的FAAs在对虾体内具有渗透压调节作用相吻合,然而具体到每种FAAs又有所不同。McCoid等(1984)认为,日本对虾(Marsupenaeu japonicus)中Gly、Pro和Ala是主要的渗透压调节剂,Fang等(1992)研究发现,Gly、Pro、Ala、氨及Tau在斑节对虾体内起着重要的渗透压调节作用,表明在虾蟹中发挥渗透压调控的FAAs大致相同,且又存在一定的特殊性。
在许多海洋生物中已经证实,FAAs中具有渗透压调节作用的是NEAA,随着外界盐度的升高,NEAA的含量显著增加,而EAA的含量保持稳定(McNamara et al, 2004; Hosoi et al, 2007)。本研究同样发现,NEAA的总量随盐度的升高而增加(P < 0.05),其中包括与盐度显著正相关的FAAs (Gly、Glu、Ala和Pro) (P < 0.05),而与NEAA相对的EAA,其总量变化不显著(P > 0.05),表明在三疣梭子蟹体内发挥渗透调节作用的FAAs主要为NEAA。值得注意的是,TAA的浓度在NEAA浓度随盐度上调中占很大比例(34%以上),暗示其在渗透调节中发挥重要作用。
有趣的是,本研究发现,盐度20时三疣梭子蟹体内FAAs含量较高,仅次于盐度50。已有研究表明,在等渗条件下,水生生物不需要消耗能量调节渗透压,生长速度较快,摄食量也较大,体内氨基酸合成旺盛。当外界水环境盐度高于或者低于三疣梭子蟹的等渗点时,摄食欲望降低,且需要付出一些能量来满足离子和渗透压调节的新陈代谢消耗,许多广盐类生物都具有这种特性(周裕华等, 2014; 王云峰等, 2002)。在实验过程中,同样观察到类似现象,盐度20时三疣梭子蟹摄食量大、活力较强且死亡率低。另外,隋延鸣等(2012)研究表明,三疣梭子蟹最适生长盐度为18.7–28.7,据此推测,三疣梭子蟹等渗点临近盐度20。然而,体内FAAs浓度是否与甲壳动物等渗点盐度相关尚需进一步研究证实。
王云峰, 朱鑫华. 盐度对鱼类生态生理学特征的影响.
海洋科学集刊 , 2002, 44 (5) : 151-158 ( 0) 0)
|
|
江山, 许强华. 盐度胁迫对三疣梭子蟹鳃Na+/K+-ATPase酶活的影响.
水产学报 , 2011, 35 (10) : 1475-1480 ( 0) 0)
|
|
孙颖民, 闫愚, 孙进杰. 三疣梭子蟹的幼体发育.
水产学报 , 2005, 8 (3) : 219-226 ( 0) 0)
|
|
周双林, 姜乃澄, 卢建平, 等. 甲壳动物渗透压调节的研究进展Ⅰ.鳃的结构与功能及其影响因子.
东海海洋 , 2001, 19 (1) : 44-51 ( 0) 0)
|
|
周裕华, 潘桂平, 周文玉, 等. 水体盐度对三疣梭子蟹生长及存活的影响.
湖南农业科学 , 2014 (10) : 64-66 ( 0) 0)
|
|
黄凯, 蒋焕超, 吴宏玉, 等. 盐度对凡纳滨对虾肌肉中游离氨基酸含量的影响.
海洋渔业 , 2010 (4) : 422-426 ( 0) 0)
|
|
梁萌青, 王士稳, 王家林, 等. 不同盐度对凡纳滨对虾血淋巴及肌肉游离氨基酸组成的影响.
渔业科学进展 , 2009, 30 (2) : 34-39 ( 0) 0)
|
|
隋延鸣, 高保全, 刘萍, 等. 三疣梭子蟹"黄选1号"盐度耐受性及适宜生长盐度分析.
大连海洋大学学报 , 2012, 27 (5) : 398-401 ( 0) 0)
|
|
潘鲁青, 刘泓宇. 甲壳动物渗透调节生理学研究进展.
水产学报 , 2005, 29 (1) : 109-114 ( 0) 0)
|
|
戴爱云, 冯钟琪, 宋玉枝, 等. 三疣梭子蟹渔业生物资源的初步调查.
动物学杂志 , 1977 (2) : 30-33 ( 0) 0)
|
|
戴爱云, 杨思谅, 宋玉枝, 等.
中国海洋蟹类. 北京: 海洋出版社, 1986 : 213 -214.
( 0) 0)
|
|
Boone WR, Claybrook DL. The effect of low salinity on amino acid metabolism in the tissues of the common mud crab, Panopeus herbstii (Milne-Edwards).
Comp Biochem Physiol A: Physiol , 1977, 57 (1) : 99-106 DOI:10.1016/0300-9629(77)90357-7 ( 0) 0)
|
|
Clark ME. A survey of the effect of osmotic dilution on free amino acids of various polychaetes.
Biol Bull , 1968, 134 (2) : 252-260 DOI:10.2307/1539601 ( 0) 0)
|
|
Dalla-Via GJ. Salinity responses of the juvenile penaeid shrimp Penaeus japonicus: II. Free amino acids.
Aquaculture , 1986, 55 (4) : 307-316 DOI:10.1016/0044-8486(86)90171-7 ( 0) 0)
|
|
Fang LS, Tang CK, Lee DL. Free amino acid composition in muscle and hemolymph of the prawn Penaeus monodon in different salinities.
Bull Jap Soc Fish Sci , 1992, 58 (6) : 1095-1102 DOI:10.2331/suisan.58.1095 ( 0) 0)
|
|
Gerard JF, Gilles R. The free amino-acid pool in Callinectes sapidus (Rathbun) tissues and its role in the osmotic intracellular regulation.
J Exp Mar Biol Ecol , 1972, 10 (2) : 125-136 DOI:10.1016/0022-0981(72)90098-6 ( 0) 0)
|
|
Hosoi M, Shinzato C, Takagi M, et al. Taurine transporter from the giant Pacific oyster Crassostrea gigas: function and expression in response to hyper-and hypo-osmotic stress.
Fish Sci , 2007, 73 (2) : 385-394 DOI:10.1111/fis.2007.73.issue-2 ( 0) 0)
|
|
Lv J, Liu P, Wang Y, et al. Transcriptome analysis of Portunus trituberculatus in response to salinity stress provides insights into the molecular basis of osmoregulation.
PLoS One , 2013, 8 (12) : e82155 DOI:10.1371/journal.pone.0082155 ( 0) 0)
|
|
McCoid V, Miget R, Finne G. Effect of environmental salinity on the free amino acid composition and concentration in penaeid shrimp.
J Food Sci , 1984, 49 (2) : 327-330 DOI:10.1111/jfds.1984.49.issue-2 ( 0) 0)
|
|
McNamara JC, Rosa JC, Greene LJ, et al. Free amino acid pools as effectors of osmostic adjustment in different tissues of the freshwater shrimp Macrobrachium olfersii (Crustacea, Decapoda) during long-term salinity acclimation.
Mar Freshwat Behav Physiol , 2004, 37 (3) : 193-208 DOI:10.1080/10236240400006208 ( 0) 0)
|
|
Shewbart KL, Mies WL, Ludwig PD. Identification and quantitative analysis of the amino acids present in protein of the brown shrimp Penaeus aztecus.
Mar Biol , 1972, 16 (1) : 64-67 DOI:10.1007/BF00347849 ( 0) 0)
|



