2. 青岛海洋科学与技术国家实验室 海洋渔业科学与食物产出过程功能实验室 青岛 266071;
3. 山东省渔业技术推广站 济南 250013
2. Laboratory for Marine Fisheries Science and Food Production Processes, Qingdao National Laboratory for Marine Science and Technology, Qingdao 266071;
3. Shandong Province Fisheries Technology Extension Station, Jinan 250013
在高等哺乳动物中,关于膜孕激素受体(mPRs)组织表达和生理学作用研究较多,而对低等脊椎动物膜孕激素受体表达特征和组织定位研究较少(Hasegawa et al, 2005; Zhu et al, 2008; 史宝等, 2013)。孕激素参与繁殖的所有环节,但在繁殖相关器官卵巢、精巢和脑等的作用机制尚不清楚,多种受体参与孕激素信号传导,并且由于高等动物的生殖系统复杂,使得相关的研究不易于开展(Mulac-Jericevic et al, 2004; Fernandes et al, 2005)。牙鲆(Paralichthys olivaceus)人工繁育技术成熟、怀卵量大,是研究孕激素调控繁殖机制很好的实验材料。鱼类卵母细胞在卵黄生成阶段完成后体积增大,停滞在有丝分裂前期。大量分泌的促性腺激素刺激卵巢滤泡细胞释放成熟诱导类固醇激素即孕激素,孕激素促使鱼类卵母细胞减数分裂重新开始,与膜孕激素受体结合,促进卵母细胞成熟(Nagahama et al, 2008)。
膜孕激素受体具有和G蛋白偶联受体(GPCRs)相似的跨膜结构域,但是,膜孕激素受体属于孕激素脂联素受体家族(PAQR)成员(Tang et al, 2005)。孕激素相关的膜受体主要包括膜孕激素受体(mPRα、mPRβ和mPRγ)和孕酮受体膜组成部分(PGMRCs)等,该受体家族在诱导鱼类和两栖类卵母细胞成熟、哺乳动物分娩等过程中发挥重要作用(Karteris et al, 2006; Josefsberg Ben-Yehoshua et al, 2007)。在牙鲆中,文献曾报道了PAQR家族一个新成员(mPR-Like, mPRL);组织特异性表达分析显示,mPRL mRNA在牙鲆卵巢、精巢、脑等繁殖相关器官表达丰富;在牙鲆精巢和卵巢发育Ⅳ期时,mPRL mRNA表达水平逐步升高并在Ⅴ期达到整个繁殖期最大值(P < 0.05),从Ⅴ期到Ⅵ期,mPRL转录水平下降,该基因相对表达量变化与性腺发育状态密切相关;但mPRL的蛋白结构和精确作用机制等仍不清楚(史宝, 20101); 李晓晓, 20132))。本研究采用实时荧光定量PCR (qRT-PCR)、免疫印迹和免疫组织化学方法,在mRNA和蛋白质水平揭示牙鲆mPRL的表达特性和细胞学定位,为揭示牙鲆mPRL的表达特征、探讨其调控卵母细胞成熟机制提供科学依据。
1) Shi B. Study on the molecular mechanisms of reproductive endocrinology in Paralichthys olivaceus and Paralichthys lethostigma. Doctoral Dissertation of Ocean University of China, 2010, 1-176 [史宝.牙鲆繁殖内分泌分子机理研究.中国海洋大学博士研究生学位论文, 2010, 1-176]
2) Li XX. Study on the physiological function of membrane progestin receptor in the reproductive cycle of flatfish. Master’s Thesis of Shanghai Ocean University, 2013, 1-73 [李晓晓.膜孕激素受体在鲆鲽类繁殖周期中的生理功能研究.上海海洋大学硕士研究生学位论文, 2013, 1-73]
1 材料与方法 1.1 实验鱼和组织准备实验用牙鲆雌鱼采自山东青岛忠海水产有限公司,为野生亲鱼自然产卵后人工育苗得到的健康苗种,经室内人工养殖达到性成熟的F1代亲鱼。牙鲆雌鱼全长为40-60 cm,体重为1428.7-2508.3 g。其培育条件:全年开放流水培育,水温为8-25℃,盐度为27-31,pH为7.8-8.4,溶解氧 > 5 mg/L。在牙鲆繁殖季节,挑选腹部膨大、松软的亲鱼,使用MS-222麻醉雌鱼后解剖。按照牙鲆卵巢发育的组织学特征,在显微镜下将卵母细胞按时相分类取样,从发育Ⅴ期卵巢分离到Ⅱ时相、Ⅲ时相、Ⅳ时相和Ⅴ时相卵母细胞,用液氮将卵母细胞速冻并在-80℃保存,用于总RNA提取。雌鱼麻醉后解剖,留取各组织样品,在4℃条件下,4%多聚甲醛[溶于0.01 mol/L磷酸盐缓冲液(PBS)中]固定20 h,梯度甲醇(25%、50%、75%和100%甲醇溶于0.01 mol/L PBS)脱水,在-20℃保存于甲醇中的样品,一部分用于免疫组化,一部分用于原位杂交;部分性腺组织用Davidesons AFA固定,用于检验性腺发育状况;使用液氮速冻后保存在-80℃的组织样品,用于总蛋白的提取。
1.2 实时荧光定量PCR检测对牙鲆mPRL mRNA在不同发育阶段卵母细胞的表达进行分析。每个卵母细胞发育时相设置4个重复,分别提取Ⅱ时相、Ⅲ时相、Ⅳ时相、Ⅴ时相和Ⅵ时相卵母细胞的总RNA,进行反转录,并使用PrimerScriptTM RT reagent Kit with gDNA Eraser试剂盒(TaKaRa, 日本)合成cDNA第1链,用于基因表达分析。使用β-actin基因作为qRT-PCR的内参基因。牙鲆mPRL引物序列为:5′-CAATCAACGAGGGTGCGTAAG-3′(mPRLF)和5′-AAAGAGAACGGCTTGGTCACTG-3′ (mPRLR);β-actin引物序列为:5′-GAAATCGCCGCACTGGTT-3′(β-actinF)和5′-GCCCATACCCACCATCACTC-3′(β-actinR)。qRT-PCR反应体系(20 μl):1 μl cDNA模版,1.5 μl引物(10 μmol/L),10 μl SYBR Premix Ex TaqTMⅡ和6 μl dH2O。采用两步法PCR扩增程序,反应条件:95℃预变性30 s,95℃ 5 s,60℃ 18 s共40个循环。qRT-PCR反应及信息的收集都在Mastercycler ep realplex实时定量PCR仪(Eppendorf, 德国)上进行。程序运行完成后进行熔解曲线(Melting curve)分析以确定引物及反应是否正常。每个样品设置3个平行孔,重复3次实验,同时设阴性对照,以确认实验结果的可靠性。
1.3 原位杂交(ISH)使用正向引物(5′-AAGCTTAGACACCGAGGTTCCCGCTTAT-3′)和反向引物(5′-GAATTCGAGGATGGTGGCAACAGGCA-3′),扩增牙鲆mPRL基因(GenBank Accession No. KM507040),获得440 bp的cDNA片段。以此为模板,使用地高辛试剂盒(Roche, 瑞士)体外转录合成正义和反义RNA探针。牙鲆卵巢和脑组织在4%多聚甲醛中固定,经脱水、透明、包埋、切片。切片经二甲苯处理2次,每次5 min,酒精梯度处理,每次5 min。PBST冲洗3次,每次10 min。蛋白酶K (10 μg/ml) 37℃消化10 min。PBST冲洗2次,每次5 min。用预杂交液70℃处理3 h,然后加入含有地高辛标记的RNA探针的杂交液,70℃杂交12 h。2×SSC洗涤,70℃孵育15 min;0.2×SSC,70℃孵育1 h。1×MAB室温洗涤5 min。血清室温封闭6 h。1:500封闭液稀释的抗体4℃孵育过夜。PBST室温冲洗6次,每次15 min;碱性磷酸缓冲液室温洗涤(2次)每次10 min。加20 μl显色液(BCIP/NBT)室温避光显色。PBST洗涤5次,每次5 min,终止反应。4%PFA-PBS固定10 min,PBST洗3次,每次5 min;酒精梯度脱水、二甲苯透明,封片,使用Nikon E80i显微镜观察并拍照。
1.4 Western blotting分析牙鲆mPRL蛋白序列,选择抗原表位,合成相应的免疫多肽;多肽常规免疫新西兰大白兔,制备抗体。冻存的牙鲆卵巢、脑、头肾、肾和肝组织(约100 mg),各加入1 ml动物组织蛋白提取试剂,匀浆、提取组织蛋白。12% SDS-PAGE电泳检测所提取的蛋白,并使用蛋白测定试剂盒测定组织总蛋白浓度。统一蛋白上样量为40 μg。蛋白提取液经12% SDS-PAGE胶分离,电转移到PVDF膜上,PBST洗涤(2次)每次5 min,以5%脱脂奶粉封闭。一抗用制备的牙鲆mPRL多克隆抗体,稀释度为1:2000;二抗用辣根过氧化物酶标记山羊抗兔IgG,稀释度为1:2000。DAB显色,凝胶成像系统拍照。使用软件对每个泳道的蛋白条带光密度值进行分析。
1.5 免疫组化组织切片脱蜡复水,3% H2O2室温孵育15 min,PBST洗涤2次,每次15 min;3% BSA室温孵育1 h,封闭非特异性反应。滴加牙鲆mPRL抗体,稀释度为1:1000,湿盒中室温孵育过夜,PBST洗涤5次,每次5 min。利用羊抗兔IgG (1:1000)作为阴性对照,孵育方法相同,室温孵育1 h。DAB显色1-2 min。苏木精复染、脱水、透明、封片,使用Nikon E80i显微镜观察并拍照。
1.6 统计分析基因表达实验所得数据用相对定量的2-△△CT方法(Livak et al, 2001)计算后,使用SPSS 17.0软件的单因素方差分析(One-way ANOVA)进行数据处理。P < 0.05为差异显著。相对表达量数据均表示为平均值±标准误(Mean±SE),并制成柱状图。蛋白表达水平检测采用AIC.AlphaView成像分析系统(Cell Biosciences Inc)分析灰度值,并制成柱状图。
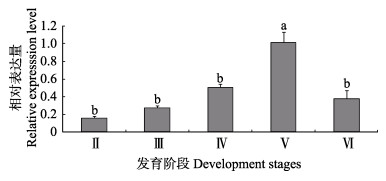
2 结果 2.1 卵子形成过程中mPRL的时序表达qRT-PCR的结果显示,在牙鲆卵巢发育Ⅴ期,mPRL基因在卵母细胞不同发育阶段均有表达,但其表达量有显著差异。mPRL基因的表达水平从Ⅱ时相到Ⅴ时相卵母细胞持续显著升高,而在Ⅵ时相卵母细胞表达水平迅速下降(P < 0.05)。mPRL基因在卵母细胞成熟阶段表达水平达到峰值,这表明mPRL基因参与卵母细胞的成熟过程(图 1)。
|
图 1 mPRL mRNA在牙鲆不同时相卵母细胞的表达 Figure 1 Relative expression levels of mPRL mRNA at various stages of oogenensis (n=4) 不同字母表示差异显著(P < 0.05),下同 Different letters indicated significant different (P < 0.05), the same as below |
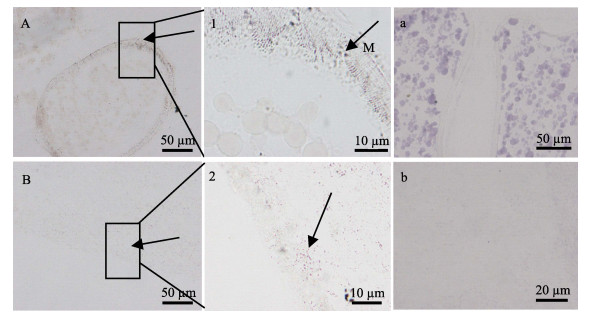
原位杂交分析mPRL mRNA在牙鲆繁殖相关组织中的细胞学定位结果显示,在卵巢和脑组织有明显的杂交信号(图 2)。在牙鲆发育成熟的卵巢中,mPRL mRNA在卵母细胞膜上表达丰富(图 2-A),将该区域放大,可观察到较强的阳性信号(图 2-1),预示了其作为膜受体行使生理功能。在牙鲆脑组织中,mPRL mRNA在脑组织神经元表达(图 2-B),局部放大后显示阳性信号较强(图 2-2)。图 2-a和图 2-b为相应组织原位杂交分析的阴性对照。
|
图 2 牙鲆mPRL基因在卵巢和脑组织中的细胞学定位 Figure 2 Localization of mPRL mRNA in ovary and brain tissues of P. olivaceus using in situ hybridization A:卵巢;1:卵巢(×1000);a:卵巢对照组;B:脑;2:脑(×1000);b:脑对照组;M:卵母细胞膜;箭头指向为阳性信号位置 A: Ovary; 1: Ovary (×1000); a: Negative control of ovary; B: Brain; 2: Brain (×1000); b: Negative control of brain; M: Oocyte membrane; the arrows indicated the positive reaction |
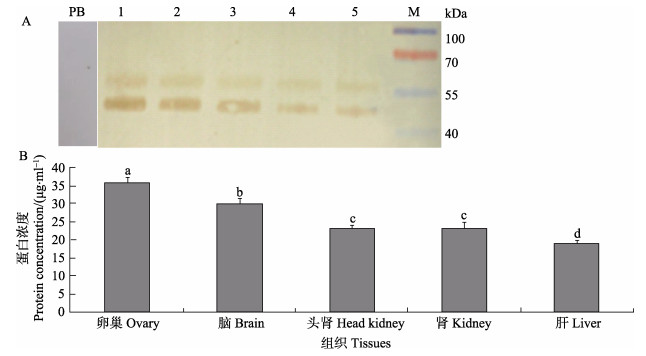
通过Western blotting方法检测牙鲆mPRL蛋白在不同组织的表达水平。结果显示,在卵巢、脑、头肾、肾脏和肝脏检测到蛋白条带,分子量约为50 kDa,比理论值(40 kDa)大(图 3-A)。对照组采用多肽抗原进行Western blotting,证实了抗体特异性。牙鲆mPRL蛋白表达量在卵巢和脑中相对较高,在头肾、肾脏和肝脏组织中也有表达,但表达量相对较少(图 3-B)。在卵巢、脑和肝脏等多个组织的表达说明,mPRL在牙鲆多种组织中参与调节孕激素生理功能。
|
图 3 牙鲆各组织mPRL蛋白的表达 Figure 3 Expression of mPRL protein in different tissues of P. olivaceus A:mPRL蛋白表达电泳图;B:mPRL蛋白表达量化;1:卵巢;2:脑;3:头肾;4:肾;5:肝;M:蛋白分子量标准;PB:阴性对照 A: Electrophoregram of protein expression of mPRL; B: Quantitative abundance of mPRL protein expression; 1: Ovary; 2: Brain; 3: Head kidney; 4: Kidney; 5: Liver; M: Protein molecular weight marker; PB: Negative control |
免疫组化结果显示,牙鲆mPRL在卵巢和脑的细胞学定位与mPRL mRNA一致。在性成熟卵巢组织中,mPRL主要分布于卵母细胞膜上,具有较强的免疫阳性显色(图 4-A);放大1000倍后可以很明显看出其在膜附近的表达密集(图 4-1)。在脑组织中mPRL主要定位在脑组织的神经元附近(图 4-B),放大1000倍后可以明显看到该区域免疫阳性反应特征(图 4-2)。图 4-a和图 4-b为相应组织免疫组化分析的阴性对照。

|
图 4 牙鲆mPRL蛋白在卵巢和脑组织的细胞定位 Figure 4 Localization of mPRL protein in the ovary and brain of P. olivaceus demonstrated by immunohistochemistry A:卵巢;1:卵巢(×1000);a:卵巢对照组;B:脑;2:脑(×1000);b:脑对照组;M:卵母细胞膜;箭头指向为阳性信号位置 A: Ovary; 1: Ovary (×1000); a: Negative control of ovary; B: Brain; 2: Brain (×1000); b: Negative control of brain; M: Oocyte membrane; the arrows indicated the positive reaction |
通过qRT-PCR方法分析了mPRL转录本在牙鲆不同组织中的表达,发现mPRL在卵巢、脑、心、鳃等组织表达丰富,在垂体、肝、肾脏、肌肉等器官相对表达量较低(李晓晓等, 2013)。为进一步分析mPRL在牙鲆卵巢的作用机制,本研究通过qRT-PCR方法检测不同发育阶段卵母细胞母源的mPRL转录本。发现mPRL mRNA随着卵母细胞发育,表达水平逐步升高;在牙鲆发育Ⅴ期的卵巢,处于Ⅴ时相卵母细胞的mPRL mRNA表达量最高。当前,关于PAQR基因家族在配子发育早期的生理作用未见研究报道(Tokumoto et al, 2006; 柳学周等, 2015)。根据本研究结果,推测mPRL可能参与卵母细胞的卵黄发生。在卵黄生成后期卵母细胞和成熟阶段卵母细胞mPRLmRNA转录水平急剧上升,预示牙鲆mPRL基因参与调控卵母细胞成熟。
3.2 表达与定位分析Western blotting分析发现,mPRL蛋白表达量在卵巢和脑中相对较高,在肝脏、肾脏、头肾中也有表达,但表达量相对较少。明显的蛋白免疫反应条带出现在约50 kDa位置,比理论预测的蛋白分子量(40 kDa)大10 kDa。这种差异可能来自糖基化作用等蛋白质翻译后的修饰(Jiménez-Castaño et al, 2007),这也是需要进一步研究证实的内容之一。在本研究中,牙鲆mPRL基因和蛋白在繁殖内分泌相关组织表达较为丰富,并且在Ⅴ时相卵母细胞mPRL mRNA表达量和Ⅴ期的卵巢组织mPRL蛋白表达量均最大,说明mPRL在卵巢具有重要的成熟调控功能。
采用原位杂交和免疫组化方法分析了牙鲆mPRL转录本和蛋白在繁殖相关器官的细胞学定位,结果显示,mPRL基因和蛋白阳性信号特异性的定位在成熟性腺的卵母细胞膜上,并在脑组织的神经元细胞中分布;mPRL在这些繁殖相关器官的分布表明,孕激素在牙鲆卵巢和脑可以通过mPRL介导的信号通路发挥作用。孕激素在神经系统具有重要的生理功能,如调节促性腺激素释放激素(GnRH)释放和繁殖行为等(Petersen et al, 2013)。mPRL在牙鲆脑的分布预示mPRL介导孕激素参与神经内分泌功能调节,进而影响牙鲆繁殖。研究发现,在牙鲆繁殖周期性腺发育的不同阶段,mPRL mRNA在脑-垂体-性腺轴相对表达水平显著升高并在Ⅴ期达到峰值(P < 0.05),在Ⅵ期表达量下降;另外,牙鲆血清中孕激素含量变化也随着性腺的发育呈先升高后降低的变化特征(史宝, 20101); 李晓晓, 20132))。因此,mPRL在牙鲆卵巢发育的过程表达增强,结合本研究中mPRL在成熟卵母细胞膜上的定位,预示mPRL是受孕激素调控的介导卵母细胞成熟的膜受体。相关的研究也发现与本研究相似的结果,通过原位杂交和免疫组化的方法发现斑马鱼(Danio rerio)的mPRα定位在卵母细胞膜附近或者卵母细胞膜上,结合云纹犬牙石首鱼(Cynoscion nebulosus)过表达mPRα可以加速卵母细胞成熟,表明mPRα参与卵母细胞成熟调控(Hanna et al, 2009; Thomas et al, 2007)。牙鲆mPRL与其他鱼类的mPRα在卵母细胞膜上类似的表达模式表明,它们可能在卵巢具有相似的生理功能。
1) Shi B. Study on the molecular mechanisms of reproductive endocrinology in Paralichthys olivaceus and Paralichthys lethostigma. Doctoral Dissertation of Ocean University of China, 2010, 1-176 [史宝.牙鲆繁殖内分泌分子机理研究.中国海洋大学博士研究生学位论文, 2010, 1-176]
2) Li XX. Study on the physiological function of membrane progestin receptor in the reproductive cycle of flatfish. Master’s Thesis of Shanghai Ocean University, 2013, 1-73 [李晓晓.膜孕激素受体在鲆鲽类繁殖周期中的生理功能研究.上海海洋大学硕士研究生学位论文, 2013, 1-73]
mPRL基因属于膜孕激素受体家族的一员,为本团队近年来在鲆鲽类发现的一种介导卵母细胞成熟的功能基因(柳学周等, 2015),并发现在半滑舌鳎(Cynoglossus semilaevis)和大黄鱼(Larimichthys crocea)等鱼类的基因组中存在该基因的同源序列;有关mPRL基因与膜孕激素受体成员mPR (α、β、γ)在介导卵母细胞成熟、神经内分泌调控和繁殖行为等方面是如何协调配比调控孕激素发挥生理学作用以及是否激活相同的信号通路发挥生理功能的研究未见报道;鉴于mPRL基因在鲆鲽类卵母细胞成熟过程中的重要作用,今后将通过真核表达方式获得重组蛋白,进一步分析其蛋白结构、家族各成员之间的作用并将产生的蛋白应用于亲鱼的促熟实验,以利于获得足够数量的和高质量具有受精能力的鱼卵,这不仅对具有经济价值的鱼类产业发展有极大的促进作用,而且可将该技术应用于濒危鱼类繁衍后代。
| Fernandes MS, Pierron V, Michalovich D, et al. Regulated expression of putative membrane progestin receptor homologues in human endometrium and gestational tissues. Journal of Endocrinology , 2005, 187 (1) : 89-101 DOI:10.1677/joe.1.06242 | |
| Hanna RN, Zhu Y. Expression of membrane progestin receptors in zebrafish (Danio rerio) oocytes, testis and pituitary. General and Comparative Endocrinology , 2009, 161 (1) : 153-157 DOI:10.1016/j.ygcen.2008.10.006 | |
| Hasegawa J, Yanaihara A, Iwasaki S, et al. Reduction of progesterone receptor expression in human cumulus cells at the time of oocyte collection during IVF is associated with good embryo quality. Human Reproduction , 2005, 20 (8) : 2194-2200 DOI:10.1093/humrep/dei005 | |
| Jiménez-Castaño L, Villamiel M, López-Fandiño R. Glycosylation of individual whey proteins by Maillard reaction using dextran of different molecular mass. Food Hydrocolloids , 2007, 21 (3) : 433-443 DOI:10.1016/j.foodhyd.2006.05.006 | |
| Josefsberg Ben-Yehoshua L, Lewellyn AL, Thomas P, et al. The role of Xenopus membrane progesterone receptor β in mediating the effect of progesterone on oocyte maturation. Molecular Endocrinology , 2007, 21 (3) : 664-673 DOI:10.1210/me.2006-0256 | |
| Karteris E, Zervou S, Pang Y, et al. Progesterone signaling in human myometrium through two novel membrane G protein coupled receptors: Potential role in functional progesterone withdrawal at term. Molecular Endocrinology , 2006, 20 (7) : 1519-1534 DOI:10.1210/me.2005-0243 | |
| Liu XZ, Shi B, Li XX, et al. Molecular characterization of the novel membrane progestin receptor gene and its role during ovarian development in the half smooth tongue sole Cynoglossus semilaevis Günther. Journal of Fishery Sciences of China , 2015, 22 (4) : 608-619 [柳学周, 史宝, 李晓晓, 等. 半滑舌鳎新型膜孕激素受体基因分子特征及其在卵巢发育过程的作用. 中国水产科学 , 2015, 22 (4) : 608-619] | |
| Livak KJ, Schmittgen TD. Analysis of relative gene expression data using real-time quantitative PCR and the 2−ΔΔCt method. Methods , 2001, 25 (4) : 402-408 DOI:10.1006/meth.2001.1262 | |
| Mulac-Jericevic B, Conneely OM. Reproductive tissue selective actions of progesterone receptors. Reproduction , 2004, 128 (2) : 139-146 DOI:10.1530/rep.1.00189 | |
| Nagahama Y, Yamashita M. Regulation of oocyte maturation in fish. Development, Growth and Differentiation , 2008, 50 (S1) : 195-219 | |
| Petersen SL, Intlekofer KA, Moura-Conlon PJ, et al. Novel progesterone receptors: Neural localization and possible functions. Frontiers in Neuroscience , 2013, 7 : 1-7 | |
| Shi B, Li XX, Liu XZ, et al. Molecular cloning and tissue expression analysis of membrane progestin receptor alpha gene (mPR α) from half smooth tongue sole Cynoglossus semilaevis Günther. Progress in Fishery Sciences , 2013, 34 (3) : 61-67 [史宝, 李晓晓, 柳学周, 等. 半滑舌鳎膜孕激素受体基因克隆与组织表达分析. 渔业科学进展 , 2013, 34 (3) : 61-67] | |
| Tang YT, Hu T, Arterburn M, et al. PAQR proteins: Novel membrane receptor family defined by an ancient 7-transmembrane pass motif. Journal of Molecular Evolution , 2005, 61 (3) : 372-380 DOI:10.1007/s00239-004-0375-2 | |
| Thomas P, Pang Y, Dong J, et al. Steroid and G protein binding characteristics of the seatrout and human progestin membrane receptor alpha subtypes and their evolutionary origins. Endocrinology , 2007, 148 (2) : 705-718 DOI:10.1210/en.2006-0974 | |
| Tokumoto M, Nagahama Y, Thomas P, et al. Cloning and identification of a membrane progestin receptor in goldfish ovaries and evidence it is an intermediary in oocyte meiotic maturation. General and Comparative Endocrinology , 2006, 145 (1) : 101-108 DOI:10.1016/j.ygcen.2005.07.002 | |
| Zhu Y, Hanna R, Schaaf M, et al. Candidates for membrane progestin receptors-past approaches and future challenges. Comparative Biochemistry Physiology Part C: Toxicology and Pharmacology , 2008, 148 (4) : 381-389 DOI:10.1016/j.cbpc.2008.05.019 |



