2. 上海海洋大学水产与生命学院 上海 201306
2. College of Fisheries and Life Science, Shanghai Ocean University, Shanghai 201306
水产品是人类优质动物蛋白的重要来源。我国是世界上最大的水产动物养殖国,产量已连续多年位居世界首位。在多年的高速发展过程中,制约养殖产业健康可持续发展的不利因素逐渐显现出来,对水产养殖业的产量和效益造成严重影响。在众多传染性病害中,病毒性疾病所造成的影响尤为严重。隶属于虹彩病毒科(Iridoviridae)的淋巴囊肿病毒为重要病原之一,该病毒粒子正面观为六角形的正二十面体构造,因所依赖的宿主细胞不同,病毒粒子大小有差异,直径介于130~350 nm之间,由核心体、中间脂质层和衣壳三部分组成(Paperna et al, 2001; Anders, 1989)。目前,淋巴囊肿病毒呈世界性分布,造成9目42科125种以上鱼类感染此病,其中,海水鱼占30科(Wolf, 1988)。病鱼在身体躯干、口等部位可见不同形状的囊肿物,虽致死率不高,但使患病鱼失去商品价值(侯吉伦等, 2017)。
牙鲆(Paralichthys olivaceus)为底栖冷水性鱼类,具有生长迅速、肉质鲜美、营养价值高、适宜集约化工厂养殖等特点,已成为我国北方的主要海水鱼类增养殖品种之一(司飞等, 2017)。1997年,我国养殖的牙鲆首次出现淋巴囊肿病,并逐渐成为危害牙鲆养殖业的重要疾病之一。针对牙鲆淋巴囊肿病,国内外学者开展了大量的研究,并取得了相应的研究进展(Fuji et al, 2006; Zheng et al, 2010; Hwang et al, 2011; Fan et al, 2014; Wu et al, 2015、2018)。为了在我国选育牙鲆抗淋巴囊肿新品种以及在分子层面解析抗病机理,作者在前期利用高通量测序技术对淋巴囊肿抗病和患病牙鲆头肾组织进行了转录组分析,筛选获得了包括efhd2和tbc1d25在内的一批和抗病性紧密相关的功能基因。
EF-hand蛋白结构域D2(EF-hand domain-containing protein D2, EFHD2),又称为Swiprosin-1,是一个高度保守的钙结合蛋白,属于EF-hand结构域家族,位于细胞膜脂肪微区域(Vuadens et al, 2004)。EFHD2在其C-端有1个保守的卷曲螺旋结构域,为蛋白质–蛋白质相互作用所必需的; 在N-末端,则具有独特的多聚丙氨酸基序(大小为6~9个丙氨酸)。EFHD2广泛表达于包括B细胞、CD4+/CD8+T细胞、自然杀伤细胞和外周血单个核细胞等各类细胞,在免疫调控起到重要的调控作用(Vega, 2016)。EFHD2可通过调节适应性和先天性免疫受体信号的关键因子Src激酶的活性而参与免疫细胞活化(Kroczek et al, 2010);调节未成熟B细胞的寿命和BCR信号阈值; 同时,作为NF-kappa-B信号通路的负调节因子,通过bcl2l1丰度的调节实现自发性凋亡的调控(Avramidou et al, 2007; Kim et al, 2013)。
TBC1D25(TBC1 domain family member 25),又称为OATL1,属于TBC家族,含有一段长约200个氨基酸的保守TBC(Rab-GAP)结构域。TBC结构域蛋白通过特异性识别Rab小GTP酶参与到细胞信号传导、肿瘤形成及细胞内其他的活动(Fukuda, 2011)。TBC1D25被鉴定为一种新的Atg8同源结合蛋白,通过与Atg8同系物直接相互作用被招募至自噬体(Itoh et al, 2011)。同时,作为Rab33B(一种结合Atg16L1的Rab蛋白)的GTP酶激活蛋白过表达促进GTP酶RAB33B从GTP结合蛋白向GDP结合蛋白的平衡,进而调节自噬体和溶酶体之间的融合来延迟自噬体的成熟,从而实现抑制自噬的作用(Itoh et al, 2017; Corona et al, 2018)。
鉴于efhd2和tbc1d25在免疫调控中的重要作用,本研究首先利用RACE法(Rapid-amplification of cDNA ends)克隆了牙鲆efhd2和tbc1d25的cDNA全序列,并对序列特征进行了生物信息学分析,同时,通过荧光定量PCR技术,研究了它们在牙鲆淋巴囊肿抗病和患病个体各组织、胚胎发育不同阶段的表达特征,以期为阐明efhd2和tbc1d25在牙鲆抗淋巴囊肿病中的作用奠定基础。
1 材料与方法 1.1 实验材料牙鲆淋巴囊肿抗病和患病个体取自中国水产科学研究院北戴河中心实验站昌黎养殖基地,体重为(235.65±73.18) g,全长为(30.49±3.17) cm。选取体表无淋巴囊肿瘤状物的3尾抗病牙鲆和有淋巴囊肿瘤状物的3尾患病牙鲆(侯吉伦等, 2017),分别取全血、鳃、肝脏、头肾、肠、性腺、肌肉、心脏和脾脏等置于液氮中速冻,48 h后置于–80℃保存备用。实验所用牙鲆不同发育时期胚胎的按照刘海金等(2008)的方法进行制备,受精卵在(16.0±0.5)℃的海水中孵化,采集受精卵(受精后0 h,下同)、4细胞(2 h)、32细胞(4 h)、128细胞(5 h)、高囊胚(6 h)、低囊胚(11 h)、原肠早期(15 h)、原肠晚期(27 h)、肌节期(32 h)、心跳期(55 h)和出膜仔鱼(62 h)样品,于液氮中速冻,48 h后置于–80℃保存备用。
1.2 RNA提取及cDNA合成采用Trizol法对本研究所需各样本的总RNA进行提取,琼脂糖凝胶电泳检测所提取总RNA质量,微量紫外分光光度计(Pultton P100+)测定RNA浓度。经检测合格后的RNA,用cDNA试剂盒(Thermo K1621)反转录获得cDNA模板。
1.3 基因全长序列的克隆根据牙鲆全基因组(Shao et al, 2017; Wei et al, 2017)和GenBank数据库中登记的牙鲆efhd2(XM_ 020089176.1)和tbc1d25(XM_020089412.1)基因序列,利用Primer Premier 6.0设计引物(efhd2-F/efhd2-R,tbc1d25-F/tbc1d25-R,表 1),以头肾cDNA为模板进行PCR扩增,验证核心片段的准确性。PCR反应体系:上下游引物各0.6 μl,模板cDNA 1 μl,PCR Mix 7.5 μl,加ddH2O至15 μl。PCR反应程序为:94℃预变性5 min; 94℃ 30 s,60℃退火30 s,72℃延伸30 s,为35个循环; 72℃延伸10 min。PCR产物经琼脂糖凝胶电泳、回收纯化,克隆至pMD18-T载体,转化至Top10感受态细胞,取3个阳性克隆进行测序。
|
|
表 1 牙鲆efhd2和tbc1d25基因序列扩增和定量PCR引物信息 Tab.1 Primers information for cloning and Q-PCR of efhd2 and tbc1d25 in Paralichthys olivaceus |
在此基础上,利用Primer Premier 6.0分别设计5'和3'端的接头引物和特异性引物(表 1),并采用RACE法,以牙鲆淋巴囊肿抗病个体头肾RNA为模板,进行降落PCR和巢式PCR。PCR产物经纯化、克隆、测序等步骤,获得5'和3'端序列。利用SnapGene 4.1软件,对所获得的5'和3'RACE序列以及中间片段进行拼接,获得efhd2和tbc1d25的cDNA全长序列。
1.4 基因的生物信息学分析氨基酸序列用ExPASy (http://www.expasy.ch/tools/dna.html)进行分析; 蛋白质结构预测使用SMART(http://smart.embl-heidelberg.de); 信号肽使用SignalP 4.1 Server (http://www.cbs.dtu.dk/services/SignalP/)进行寻找; 用TMHMM server v.2.0分析氨基酸跨膜区(http://www.cbs.dtu.dk/services/TMHMM-2.0/); 采用ClustalX2对氨基酸序列进行多重比对。使用MEGA10.0软件的Neighbor-Joining(NJ)法构建系统进化树(Bootstrap=1000)。
1.5 荧光定量PCR根据牙鲆efhd2、tbc1d25和β-actin(内参基因)基因序列,分别设计目的基因和内参的引物(表 1),并以淋巴囊肿抗病和患病个体不同组织以及胚胎发育不同时期的cDNA为模板,进行荧光定量PCR检测。定量检测采用Power SYBR Green PCR Master Mix (ABI, 美国)试剂盒在ABI 7900 PCR仪上开展。基因的相对表达量用2–ΔΔCt法分析(马慧鑫等, 2018)。所有样品均设置3个平行,结果以平均值±标准误(Mean±SE)表示,并利用SPSS 19.0软件进行单因素方差分析(One-way ANOVA) (P < 0.05)。
2 结果与分析 2.1 牙鲆efhd2与tbc1d25基因序列分析本研究克隆到的牙鲆efhd2基因cDNA全长5231 bp,其中,5'非翻译区(Untranslated region, 5'UTR)长度142 bp,3'UTR长度4390 bp。ORF长度699 bp,编码232个氨基酸,预测分子量为26.4 kDa,等电点约为5.08。牙鲆efhd2基因所编码的蛋白在第89~117以125~153位氨基酸具有2个典型的EF-hand结构域(图 1)。

|
图 1 牙鲆efhd2基因核苷酸序列及推测的氨基酸序列 Fig.1 Nucleotide and deduced amino acid sequences of P. olivaceus efhd2 方框内为起始密码子和终止密码子,阴影部分为EF-hand结构域,下划线为PolyA序列 Frames indicate the start codon and stop codon respectively, shadow region indicates the EF-hand domain, underline indicates the PolyA tail sequence |
tbc1d25基因全长为3173 bp,其中,5'UTR长度为108 bp,3'UTR长度为464 bp。ORF长度为2601 bp,编码866个氨基酸,预测分子量为96.4 kDa,等电点约为5.47。TBC1D25蛋白在199~431位氨基酸为典型的TBC结构域(图 2)。

|
图 2 牙鲆tbc1d25基因核苷酸序列及推测的氨基酸序列 Fig.2 Nucleotide and deduced amino acid sequences of P. olivaceus tbc1d25 方框内为起始密码子和终止密码子,阴影部分为TBC结构域,下划线为PolyA序列 Frames indicate the start codon and stop codon respectively, shadow region indicates the TBC domain, underline indicates the PolyA tail sequence |
SignalP分析未发现EFHD2和TBC1D25蛋白具有信号肽。TMHMM分析显示,这2个蛋白均无跨膜区。采用ExPASy网站(http://web.expasy.org/)的GOR4工具预测EFHD2与TBC1D25蛋白质的二级结构。EFHD2蛋白的α-螺旋(Alpha helix, Hh)包含150个氨基酸残基,占氨基酸残基总量的64.38%;延伸链(Extended strand, Ee)包含10个氨基酸残基,占氨基酸残基总量的4.29%;无规卷曲(Random coil, Cc)包含73个氨基酸残基,占氨基酸残基总量的31.33%。在TBC1D25蛋白中,α-螺旋包含274个氨基酸残基,占氨基酸残基总量的31.60%;延伸链包含109个氨基酸残基,占氨基酸残基总量的12.57%;无规卷曲包含484个氨基酸残基,占氨基酸残基总量的55.82%。较之于EFHD2蛋白,TBC1D25蛋白α-螺旋含量比例少,而延伸链和无规卷曲的含量比例较高。
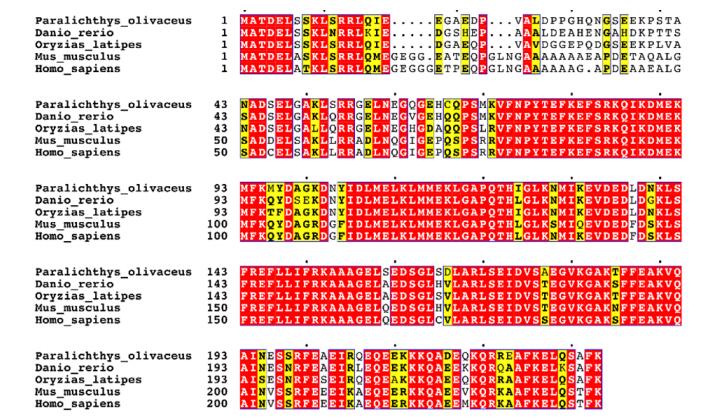
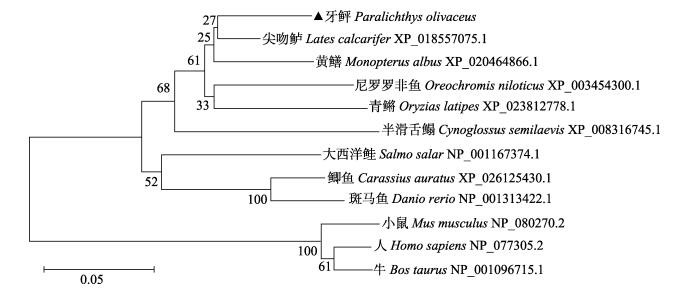
2.2 多序列比对与系统发育树分析将EFHD2蛋白分别与斑马鱼(Danio rerio)(NP_ 001313422.1)、青鳉(Oryzias latipes)(XP_023812778.1)、小鼠(Mus musculus)(NP_080270.2)和人(Homo sapiens) (NP_077305.2)的同源序列蛋白进行比较,序列一致性分别为83%、88%、73%和72%(图 3)。利用NJ法对牙鲆EFHD2蛋白与其他8个物种的EFHD2蛋白氨基酸序列进行系统进化树构建,结果显示,牙鲆EFHD2与半滑舌鳎(Cynoglossus semilaevis)聚为一小支,随后与青鳉、大西洋鲑(Salmo salar)、鲫鱼(Carassius auratus)和斑马鱼聚为一大支,而小鼠、人和牛(Bos taurus)等哺乳动物则聚为另一支(图 4)。
|
图 3 牙鲆EFHD2氨基酸多重序列比对结果 Fig.3 The multiple sequence alignment of the EFHD2 amino acid |
|
图 4 牙鲆EFHD2与其他物种EFHD2系统进化分析 Fig.4 Phylogenetic analysis of P. olivaceus EFHD2 amino acid sequence with EFHD2 sequences of other species |
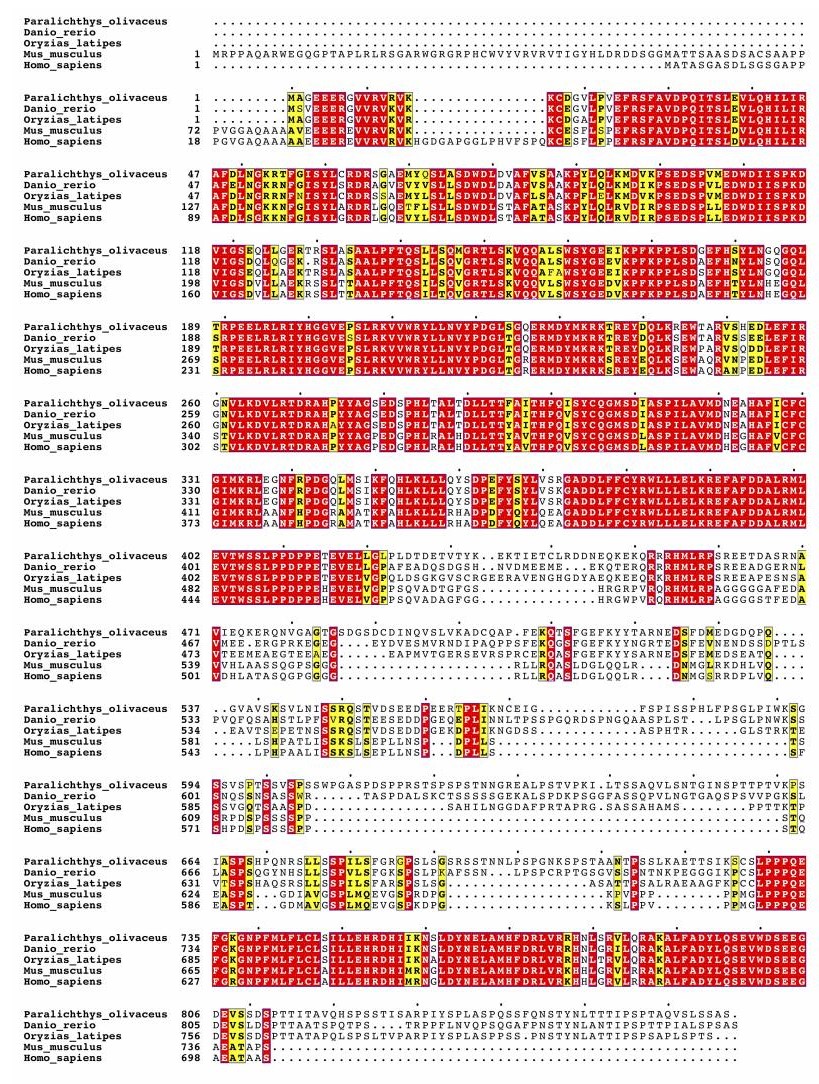
TBC1D25蛋白斑马鱼(NP_001121708.10)、青鳉(XP_011471287.2)、小鼠(NP_001159909.1)和人(NP_ 001335191.1)的同源序列一致性分别为71%、74%、72%和74%(图 5)。进化树结果表明,牛、小鼠和人等哺乳动物聚为另一支,6种鱼类聚为另一支,牙鲆在鱼类所构成的一支中,先与半滑舌鳎聚为一支,再与青鳉、大西洋鲑、鲫鱼和斑马鱼聚为一大支(图 6)。
|
图 5 牙鲆TBC1D25氨基酸多重序列比对结果 Fig.5 The multiple sequence alignment of the TBC1D25 amino acid |

|
图 6 牙鲆TBC1D25与其他物种TBC1D25系统进化分析 Fig.6 Phylogenetic analysis of P. olivaceus TBC1D25 amino acid sequence with TBC1D25 sequences of other species |
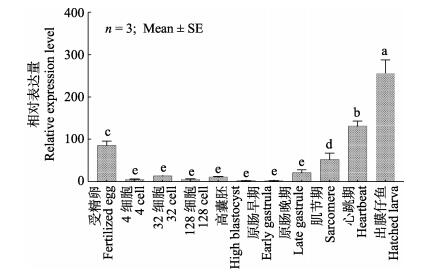
以β-actin为内参基因,利用荧光定量PCR检测了牙鲆受精卵、4细胞、32细胞、128细胞、高囊胚、低囊胚、原肠早期、原肠晚期、肌节期、心跳期和出膜仔鱼中efhd2与tbc1d25 mRNA的表达情况,并以原肠早期为基准进行相对表达量的计算。结果显示,efhd2基因在胚胎发育的各个时期均有不同程度的表达(图 7),但在4细胞、低囊胚和原肠早期的表达量相对较低,与其他时期差异显著(P < 0.05);从肌节期开始,efhd2的表达量开始呈上升趋势,且在出膜仔鱼中的表达量,显著高于其他各组(P < 0.05)。
|
图 7 牙鲆efhd2基因在胚胎发育不同时期的相对表达 Fig.7 The relative expression level of P. olivaceus efhd2 in different embryo development stage 误差线上方不同字母代表差异显著(P < 0.05),下同 Different letters above the error bars indicate significant difference (P < 0.05). The same as below |
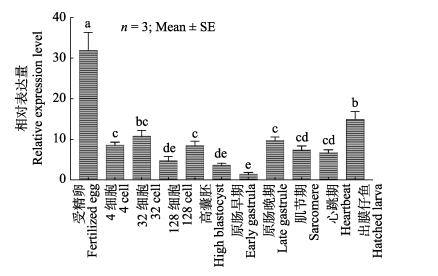
tbc1d25基因在胚胎发育的各个时期也均有不同程度的表达(图 8)。其中,受精卵中的表达量显著高于其他时期(P < 0.05);随着发育的进行,tbc1d25基因的表达量在原肠晚期降至最低(P < 0.05);在之后的发育时期中,原肠晚期、肌节期和心跳期的表达量差异不显著(P > 0.05);出膜仔鱼中tbc1d25的表达量又有一定的上升,显著高于除受精卵和32细胞之外的其他时期(P < 0.05)。
|
图 8 牙鲆tbc1d25基因在胚胎发育不同时期的相对表达 Fig.8 The relative expression level of P. olivaceus tbc1d25 in different embryo development stage |
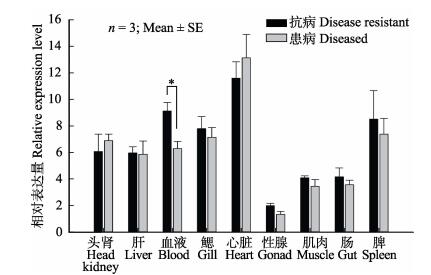
以患病组性腺为基准进行efhd2和tbc1d25基因相对表达量的计算。efhd2基因在所检测的淋巴囊肿抗病和患病个体的头肾、肝脏、血液、鳃、心脏、性腺、肌肉、肠和脾脏等组织中均有表达(图 9)。其中,在抗病鱼的血液、鳃、性腺、肌肉和脾脏的相对表达量要高于患病鱼,特别是在血液中,抗病鱼efhd2基因的表达量高于患病鱼,差异显著(P < 0.05)。
|
图 9 牙鲆efhd2基因在淋巴囊肿抗病和患病个体不同组织的相对表达 Fig.9 The relative expression level of P. olivaceus efhd2 in different tissues of lymphocystis disease resistant and sensitive individuals *为差异显著(P < 0.05) *indicates significant difference (P < 0.05) |
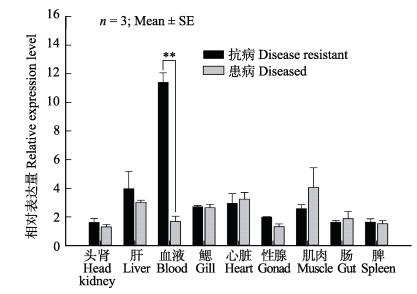
与efhd2基因相似,tbc1d25基因在所检测的各个组织中也均有表达(图 10)。其中,在抗病鱼的肝脏、血液、性腺的相对表达量要高于患病鱼,特别是在血液中的表达量,二者差异极显著(P < 0.01)。
|
图 10 牙鲆tbc1d25基因在淋巴囊肿抗病和患病个体不同组织的相对表达 Fig.10 The relative expression level of P. olivaceus tbc1d25 in different tissues of lymphocystis disease resistant and sensitive individuals **为差异极显著(P < 0.01) **indicates highly significant difference (P < 0.01) |
本研究克隆获得了牙鲆efhd2和tbc1d25基因的cDNA全序列,序列分析表明,上述2个基因都含有各自家族典型的结构域。同源性比较和系统进化树分析显示,在鱼类中,2个基因与其他鱼种具有较高的同源性,在进化上表现出一定的保守性。目前,关于efhd2和tbc1d25基因功能的研究,开展的较少,在鱼类上尚未见报道。
本文首次对efhd2和tbc1d25基因在牙鲆胚胎发育不同时期的表达模式进行了研究,在胚胎发育的各个时期,2个基因均有不同程度的表达。efhd2基因在受精卵中有一定量的表达,表明其可能为母源效应基因。其表达量在经过卵裂期到原肠晚期的低水平表达后,从肌节期开始,又显著上升。efhd2是高度保守的钙结合蛋白,在神经和免疫细胞的Ca2+信号传导中起重要作用(Brachs et al, 2013)。在牙鲆的胚胎发育中,自原肠后期开始,神经胚开始逐渐形成,神经细胞被大量生成,efhd2基因在原肠后期开始所出现的表达水平提高,可能与之有关。
在所研究的胚胎发育各时期中,tbc1d25基因在受精卵的表达量最高,表明其也是母源效应基因。tbc1d25所属的TBC基因家族是真核细胞保守的膜转运蛋白,参与膜转运的各种步骤,包括囊泡形成、沿细胞骨架的囊泡运输、运输囊泡与靶膜的锚定/对接、以及运输囊泡与靶膜的膜融合等(Pereira-Leal et al, 2001; Grosshans et al, 2006; Schwartz et al, 2007; Fukuda, 2008; Stenmark, 2009; Frasa, 2012)。而在胚胎发育的各阶段,都离不开膜转运的参与,因此,tbc1d25在此过程中可能起到一定的作用。
本研究中,牙鲆淋巴囊肿抗病个体血液中efhd2和tbc1d25基因的表达量都显著高于患病个体。鱼类免疫相关基因在血液中高表达的现象,在以往的研究中也有所报道。例如,在罗非鱼的11个组织中,血液里TRIM16和TRIM25的表达量最高(郑建美等, 2017)。血液是机体内不同器官间物质的传输介质。在牙鲆淋巴囊肿患病个体的心脏、头肾、脾脏和肠等内脏器官中均可检测到淋巴囊肿病毒颗粒(曲凌云等, 2000)。Kinne(1984)认为,鳃可能是淋巴囊肿病毒感染牙鲆的一个门户。病毒进入鳃之后,就需要通过连接各内脏器官的液体介质——血液进行传播。除了作为传输介质,血液也是重要的免疫器官,是T淋巴细胞、B淋巴细胞等各类免疫细胞的天然携带者,可在体内免疫应答过程中执行关键的生理和生化功能。随着血液流经整个机体,会将大量的免疫细胞从一个器官转移到另一个器官,从而充当免疫系统管道的角色,在鱼类疾病防治中发挥着重要的作用(Dalmo et al, 1997; Castillo et al, 1998)。就淋巴囊肿病毒感染而言,当病毒颗粒通过血液在不同器官间传输时,可能会激活血液中相关免疫细胞的免疫反应,从而导致包括efhd2和tbc1d25等在内的一系列基因的高表达。但有趣的是,efhd2的功能是促进细胞凋亡,而tbc1d25的潜在作用则是抑制自噬。细胞凋亡和自噬之间存在着复杂的调控关系,彼此之间既可相互促进(Gorski et al, 2003),也可互为拮抗(Young et al, 2006; Zeng et al, 2012; Hassan et al, 2015; Chen et al, 2016)。就本研究而言,淋巴囊肿病毒感染牙鲆后,抗病个体血液中的细胞凋亡和自噬互为拮抗关系。通过较高水平的细胞凋亡,达到对因病毒感染所损伤血液细胞的消除,从而恢复血液组成的动态平衡,这可能对维持病毒感染后鱼体的正常生理水平和实现鱼体的抗病功能具有重要的作用。
作为重要的免疫器官,头肾和脾的免疫功能已被广泛研究(Yang et al, 2016;张文婷等, 2016;郑建美等, 2017)。免疫功能基因在头肾和脾的表达量,受多种因素所影响,并不一定高于其他组织。在半滑舌鳎中,TLR5S基因在肝脏中的表达量最高,而在脾的表达量最低(张文婷等, 2016)。在本研究中,淋巴囊肿抗病和患病个体头肾和脾efhd2和tbc1d25基因的表达量差异不显著,其可能原因为efhd2和tbc1d25基因在淋巴囊肿病毒进入鱼体经血液向其他组织扩散的阶段起到免疫作用,但具体原因有待于深入研究。
综上所述,本研究报道了牙鲆efhd2和tbc1d25基因的分子特征,分析了它们不同胚胎发育过程以及淋巴囊肿抗病和患病不同组织的表达情况特征,为进一步研究二者的功能和牙鲆淋巴囊肿抗病机理奠定了一定的理论基础。
Anders K. Lymphocystis disease of fishes, in viruses of lower vertebrates. Heidelberg: Springer, 1989, 141–160
|
Avramidou A, Kroczek C, Lang C, et al. The novel adaptor protein Swiprosin-1 enhances BCR signals and contributes to BCR-induced apoptosis. Cell Death and Differentiation, 2007, 14(11): 1936-1947 |
Brachs S, Lang C, Buslei R, et al. Monoclonal antibodies to discriminate the ef hand containing calcium binding adaptor proteins EFhd1 and EFhd2. Monoclonal Antibodies in Immunodiagnosis and Immunotherapy, 2013, 32(4): 237-245 DOI:10.1089/mab.2013.0014 |
Castillo A, Razquin B, Villena AJ, et al. Thymic barriers to antigen entry during the post-hatching development of the thymus of rainbow trout, Oncorhynchus mykiss. Fish & Shellfish Immunology, 1998, 8(3): 157-170 |
Chen Z, Jin T, Lu Y. AntimiR-30b inhibits TNF-α mediated apoptosis and attenuated cartilage degradation through enhancing autophagy. Cellular Physiology and Biochemistry, 2016, 40(5): 883-894 DOI:10.1159/000453147 |
Corona AK, Jackson WT. Finding the middle ground for autophagic fusion requirements. Trends in Cell Biology, 2018, 28(11): 869-881 DOI:10.1016/j.tcb.2018.07.001 |
Dalmo RA, Ingebrigtsen K, B gwald J. Non-specific defense mechanisms in fish, with particular reference to the reticuloendothelial system (RES). Journal of Fish Diseases, 1997, 20(4): 241-273 DOI:10.1046/j.1365-2761.1997.00302.x |
Fan CX, Chen SL, Wang L, et al. Screening and identification of SSR markers associated with lymphocystis disease resistance in Japanese flounder (Paralichthys olivaceus). Journal of Fisheries of China, 2014, 38(4): 577-583 [ 范彩霞, 陈松林, 王磊, 等. 牙鲆抗淋巴囊肿病相关SSR标记的筛选与鉴定. 水产学报, 2014, 38(4): 577-583] |
Frasa MAM, Koessmeier KT, Ahmadian MR, et al. Illuminating the functional and structural repertoire of human TBC/RABGAPs. Nature Reviews Molecular Cell Biology, 2012, 13(2): 67-73 DOI:10.1038/nrm3267 |
Fuji K, Kobayashi K, Hasegawa O, et al. Identification of a single major genetic locus controlling the resistance to lymphocystis disease in Japanese flounder (Paralichthys olivaceus). Aquaculture, 2006, 254(1): 203-210 |
Fukuda M. Membrane traffic in the secretory pathway. Cellular and Molecular Life Sciences, 2008, 65(18): 2801-2813 DOI:10.1007/s00018-008-8351-4 |
Fukuda M. TBC proteins: GAPs for mammalian small GTPase Rab?. Bioscience Reports, 2011, 31(3): 159-168 DOI:10.1042/BSR20100112 |
Gorski SM, Chittaranjan S, Pleasance ED, et al. A SAGE approach to discovery of genes involved in autophagic cell death. Current Biology, 2003, 13(4): 358-363 DOI:10.1016/S0960-9822(03)00082-4 |
Grosshans BL, Ortiz D, Novick P. Rabs and their effectors: Achieving specificity in membrane traffic. Proceedings of the National Academy of Sciences, 2006, 103(32): 11821-11827 DOI:10.1073/pnas.0601617103 |
Hassan M, Selimovic D, Hannig M, et al. Endoplasmic reticulum stress-mediated pathways to both apoptosis and autophagy: Significance for melanoma treatment. World Journal of Experimental Medicine, 2015, 5(4): 206-217 DOI:10.5493/wjem.v5.i4.206 |
Hou JL, Wang GX, Zhang XY, et al. Analysis of growth and lymphocystis disease resistance of selected breeding families of Japanese flounder (Paralichthys olivaceus). Journal of Fishery Sciences of China, 2017, 24(4): 727-737 [ 侯吉伦, 王桂兴, 张晓彦, 等. 牙鲆抗淋巴囊肿病家系选育及生长和抗病性能分析. 中国水产科学, 2017, 24(4): 727-737] |
Hwang SD, Fuji K, Takano T, et al. Linkage mapping of Toll-like receptors (TLRs) in Japanese flounder, Paralichthys olivaceus. Marine Biotechnology, 2011, 13(6): 1086-1091 DOI:10.1007/s10126-011-9371-x |
Itoh T, Fukuda M. Roles of Rab-GAPs in regulating autophagy, in autophagy: Cancer, other pathologies, inflammation, immunity, infection, and aging. Cambridge: Academy Press, 2017: 143-157
|
Itoh T, Kanno E, Uemura T, et al. OATL1, a novel autophagosome- resident Rab33B-GAP, regulates autophagosomal maturation. Journal of Cell Biology, 2011, 192(5): 839-853 DOI:10.1083/jcb.201008107 |
Kim YD, Kwon MS, Na BR, et al. Swiprosin-1 expression is up-regulated through protein kinase C-θ and NF-κB pathway in T cells. Immune Network, 2013, 13(2): 55-62 |
Kinne O. Diseases of marine animals. Volume Ⅳ, Part 1, Introduction, Pisces. Hamburg: Biologische Anstalt Helgoland, 1984, 1–541
|
Kroczek C, Lang C, Brachs S, et al. Swiprosin-1/EFhd2 controls B cell receptor signaling through the assembly of the B cell receptor, Syk, and phospholipase C2 in membrane rafts. Journal of Immunology, 2010, 184(7): 3665-3676 DOI:10.4049/jimmunol.0903642 |
Liu HJ, Wang CA, Zhu XC, et al. Embryonic development of gynogenetic diploid and triploid Japanese flounder Paralichthys olivaceus. Journal of Dalian Fisheries University, 2008, 23(3): 161-167 [ 刘海金, 王常安, 朱晓琛, 等. 牙鲆单倍体, 三倍体, 雌核发育二倍体和普通二倍体胚胎发育的比较. 大连水产学院学报, 2008, 23(3): 161-167 DOI:10.3969/j.issn.1000-9957.2008.03.001] |
Ma HX, Wang L, Wang LQ, et al. The different expression patterns of the gene Arginase Ⅱ in Paralichthys olivaceus and the correlation between its expression and Edwardsiella tarda infection. Progress in Fishery Sciences, 2018, 39(3): 44-52 [ 马慧鑫, 王磊, 汪林庆, 等. 牙鲆精氨酸酶Ⅱ基因的克隆以及免疫应答表达分析. 渔业科学进展, 2018, 39(3): 44-52] |
Paperna I, Vilenkin M, Alves de Matos AP. Iridovirus infections in farm-reared tropical ornamental fish. Diseases of Aquatic Organisms, 2001, 48(1): 17-25 |
Pereira-Leal JB, Seabra MC. Evolution of the rab family of small GTP-binding proteins. Journal of Molecular Biology, 2001, 313(4): 889-901 |
Qu LY, Sun XQ, Zhang JX. Electron ultramicroscopic observation on lymphocystis disease of the left-eyed flounder Paralichthys olivaceus. Journal of Qingdao Ocean University, 2000, 30(2): 105-110 [ 曲凌云, 孙修勤, 张进兴. 养殖牙鲆淋巴囊肿病的电镜观察. 青岛海洋大学学报, 2000, 30(2): 105-110] |
Schwartz SL, Cao C, Pylypenko O, et al. Rab GTPases at a glance. Journal of Cell Science, 2007, 120(22): 3905-3910 DOI:10.1242/jcs.015909 |
Shao CW, Bao BL, Xie ZY, et al. The genome and transcriptome of Japanese flounder provide insights into flatfish asymmetry. Nature Genetics, 2017, 49(1): 119-124 DOI:10.1038/ng.3732 |
Si F, Sun ZH, Yu SS, et al. Analysis of the genetic variability of the captured population of Japanese flounder Paralichthys olivaceus in the coastal releasing area of Qinhuangdao. Progress in Fishery Sciences, 2017, 38(6): 18-24 [ 司飞, 孙朝徽, 于姗姗, 等. 秦皇岛近海增殖放流区牙鲆(Paralichthys olivaceus)回捕群体的遗传多样性分析. 渔业科学进展, 2017, 38(6): 18-24] |
Stenmark H. Rab GTPases as coordinators of vesicle traffic. Nature Reviews Molecular Cell Biology, 2009, 10(8): 513-525 DOI:10.1038/nrm2728 |
Vega IE. EFhd2, a protein linked to alzheimer's disease and other neurological disorders. Frontiers in Neuroscience, 2016, 10: 150 |
Vuadens F, Rufer N, Kress A, et al. Identification of swiprosin 1 in human lymphocytes. Proteomics, 2004, 4(8): 2216-2220 DOI:10.1002/(ISSN)1615-9861 |
Wei XL, Xu ZC, Wang GX, et al. pBACode: A random-barcode- based high-throughput approach for BAC paired-end sequencing and physical clone mapping. Nucleic Acids Research, 2017, 45(7): e52 |
Wolf K. Fish viruses and fish viral diseases. New York: Cornell University Press, 1988: 476
|
Wu R, Sheng X, Tang X, et al. Transcriptome analysis of flounder (Paralichthys olivaceus) gill in response to lymphocystis disease virus (LCDV) infection: Novel insights into fish defense mechanisms. International Journal of Molecular Sciences, 2018, 19(1): 160 DOI:10.3390/ijms19010160 |
Wu R, Tang X, Sheng X, et al. Relationship between expression of cellular receptor-27.8kDa and lymphocystis disease virus (LCDV) infection. PLoS One, 2015, 10(5): e0127940 DOI:10.1371/journal.pone.0127940 |
Yang Y, Huang YH, Yu YP, et al. RING domain is essential for the antiviral activity of TRIM25 from orange spotted grouper. Fish & Shellfish Immunology, 2016, 55: 304-314 |
Young ARJ, Chan EYW, Hu XW, et al. Starvation and ULK1-dependent cycling of mammalian Atg9 between the TGN and endosomes. Journal of Cell Science, 2006, 119(18): 3888-3900 DOI:10.1242/jcs.03172 |
Zeng R, Chen Y, Zhao S, et al. Autophagy counteracts apoptosis in human multiple myeloma cells exposed to oridonin in vitro via regulating intracellular ROS and SIRT1. Acta Pharmacologica Sinica, 2012, 33(1): 91-100 DOI:10.1038/aps.2011.143 |
Zhang WT, Xiang JS, Li HL, et al. Molecular cloning, characterization, and expression of three TLR5S splicing variants in half-smooth tongue sole. Journal of Fishery Sciences of China, 2016, 23(1): 10-20 [ 张文婷, 向晋松, 李海龙, 等. 半滑舌鳎TLR5S三种剪切型基因的克隆与表达分析. 中国水产科学, 2016, 23(1): 10-20] |
Zheng FR, Sun XQ, Xing MQ, et al. Immune response of DNA vaccine against lymphocystis disease virus and expression analysis of immune-related genes after vaccination. Aquaculture Research, 2010, 41(10): 1444-1451 |
Zheng JM, Gao FY, Lu MX, et al. Cloning and expression analysis of TRIM16 and TRIM25 genes from Nile Tilapia (Oreochromis niloticus). Journal of Agricultural Biotechnology, 2017, 25(6): 861-873 [ 郑建美, 高凤英, 卢迈新, 等. 尼罗罗非鱼TRIM16和TRIM25基因的克隆及表达分析. 农业生物技术学报, 2017, 25(6): 861-873] |



