2. 青岛海洋科学与技术试点国家实验室海洋渔业科学与食物产出过程功能实验室 青岛 266071;
3. 中国水产科学研究院黄海水产研究所 农业农村部海洋渔业可持续发展重点实验室 青岛 266071
2. Laboratory for Marine Fisheries Science and Food Production Processes, Pilot National Laboratory for Marine Science and Technology (Qingdao), Qingdao 266071;
3. Yellow Sea Fisheries Research Institute, Chinese Academy of Fishery Sciences, Key Laboratory of Sustainable Development of Marine Fisheries, Ministry of Agriculture and Rural Affairs, Qingdao 266071
C-JUN氨基末端激酶(c-Jun N-terminal kinase, JNK)在1990年被发现,是形成丝裂原活化蛋白激酶(MAPK)超家族的重要亚基。JNK基因家族具有THR-Pro-Tyr(TPY)磷酸化位点的丝氨酸/苏氨酸蛋白激酶(S_TKC)典型结构域,是上游基因MKK4与MKK7的激活区域,磷酸化的JNK可激活下游各种转录因子(Davis, 2000; Minden et al, 2008)和非转录因子(Lin, 2003),参与细胞增殖(Zhang et al, 2002)、凋亡(Kyriakis et al, 1994)、分化和免疫应激(Huang et al, 2009)等生理过程。国内外研究者发现,JNK可介导多种外界因素引起的细胞凋亡,如Dhanasekaran等(2008)研究发现,JNK可活化其下游转录因子c-JUN/AP-1的活性,进而调节凋亡蛋白的表达;活化P53基因的表达可调节细胞凋亡(Jones et al, 2008);JNK还可以介导非转录因子BCL-2家族基因的表达来调节细胞凋亡(Aoki et al, 2002)。JNK除在细胞凋亡中发挥重要作用外,在机体免疫应激过程中也发挥重要作用,如在果蝇(Drosophila)中,JNK基因可以激活脂肪体中抗菌肽基因的表达,参与对致病菌(Bond et al, 2009)、真菌(Sluss et al, 1996)和病毒(Delaney et al, 2006)的免疫防御;Shi等(2012)在凡纳滨对虾(Litopenaeus vannamei)中获得的JNK同源基因与WSSV的复制和基因转录有关;Zhu等(2016)在中华绒螯蟹(Eriocheir sinensis)中发现,JNK信号通路可调节抗菌肽(AMPs)的表达。可见JNK在机体的免疫防御过程中具有极其重要的作用。然而,在三疣梭子蟹(Portunus trituberculatus)中,有关JNK是否参与细胞凋亡、免疫防御的作用机制尚未见报道。
三疣梭子蟹具有较高的经济价值,是我国重要的海产养殖品种(任海波等, 2018)。但由于养殖环境的破坏与病害频发,三疣梭子蟹养殖规模呈现下降的趋势,其中,副溶血弧菌(Vibrio parahaemolyticus)和白斑综合征病毒(WSSV)是导致三疣梭子蟹病害频发的主要病原(周俊芳等, 2014; 李卢, 2005; 阎斌伦等, 2010)。因此,本研究采用RACE技术克隆三疣梭子蟹的JNK基因,通过生物学软件分析其基因结构与功能,并利用实时荧光定量技术(qRT-PCR)对其在不同病原感染下的表达模式进行分析,为进一步探索三疣梭子蟹JNK基因在免疫防御中的作用机制提供数据参考。
1 材料与方法 1.1 实验样品的获取三疣梭子蟹采集于山东省潍坊市昌邑海丰养殖基地,选择健康的三疣梭子蟹200只[(25±3) g],在10 m2的室内水池中暂养7 d,水温为(25±2)℃,盐度为33,持续充氧,为保证水质良好,每天换水1/3,定时、定点、定量投喂新鲜杂鱼,投喂量为其体重的30%左右。随机选取3只暂养后的健康三疣梭子蟹,分别取其10个组织(脑、肝胰腺、血细胞、肌肉、胸腺、肠、眼柄、胃、鳃和心脏)存于液氮,用于组织表达分布分析,其中,血细胞800×g 4℃离心10 min,去上清液,保留血细胞,并保存于液氮中。
将剩余的健康三疣梭子蟹平均分为3组,即对照组(甲壳动物生理盐水)、副溶血弧菌感染组(1×107 CFU/ml)和WSSV(3.7×107 copy/ml)感染组,每组50只以确保有足够的取样个体数量,浓度参照张杰等(2018),注射量为100 μl,分别在感染0、3、6、12、24、48和72 h时取其鳃、肝胰腺和血细胞组织,每组取3只混合放置在1.5 ml离心管中。其中,血细胞800×g 4℃离心10 min,去上清液,保留血细胞,并保存于液氮中,用于后续总RNA提取等。
1.2 总RNA提取与RACE模板合成将保存于液氮未处理的组织进行充分研磨,采用TRIzol® Reagent(Roche公司)方法进行总RNA提取,然后进行1%琼脂糖凝胶电泳和紫外分光光度计(NanoDrop 2000, Thermo)检测其质量和浓度,将高质量的RNA进行分装保存(–80℃)。将各组织中高质量的总RNA均匀混合,并使用SMARTer® RACE cDNA Amplification Kit (TaKaRa公司)试剂盒合成3′和5′ RACE cDNA模板(–80℃分装保存),用于后续基因克隆实验。
1.3 PtJNK基因cDNA全长扩增根据三疣梭子蟹转录组数据库筛选得到PtJNK的EST序列,利用Primer Premier 5.0软件设计3′和5′ RACE特异性引物及通用引物,由生工生物工程(上海)有限公司合成(表 1),使用Trans Taq® DNA高保真聚合酶(北京全式金生物公司)进行3′和5′末端巢式PCR扩增,第1轮使用UPM通用引物,10 µl反应体系:0.5 µl模板、0.4 µl Forward/Reverse Primer (10 µmol/L)、5 µl Premix Taq (LA Taq Ver 2.0)、ddH2O补足;程序:94℃ 5 min;94℃ 30 s,60℃ 30 s,72℃ 1.5 min,35个循环;72℃ 10 min。第2轮以第1轮反应为模板,使用NUP通用引物,20 ml反应体系,程序:94℃ 5min;94℃ 30 s,60℃ 30 s,72℃ 1.5 min,35个循环;72℃ 10 min。将获得的PCR产物使用1%琼脂糖凝胶电泳检测,将检测合理的目的条带进行切胶回收(TaKaRa Mini BEST Agarose Gel DNA Extraction Kit Ver.4.0),与pMD-18T载体(TaKaRa)连接3 h,转化至DH5α大肠杆菌感受态细胞(TSINGKE)中,涂布于含氨苄的固体培养基上,37℃恒温过夜培养,挑取阳性单克隆,加入含100 µg/ml氨苄的LB液体培养基中,37℃ 200 r/min振荡培养4 h,用M13-47/48引物进行菌落PCR鉴定,并将检测准确的目的菌液送至生工生物工程(上海)有限公司进行测序。
|
|
表 1 本研究所用引物序列 Tab.1 Nucleotide sequences of the PCR primers used in this study |
利用Contig Express软件将3′和5′克隆序列与EST序列进行拼接、验证,得到PtJNK基因的cDNA全长,利用NCBI-BLAST(http://blast.ncbi.nlm.nih.gov/Blast.cgi)在线软件对PtJNK基因序列进行比对,并使用ORF Finder (http://www.ncbi.nlm.nih.gov/projects/gorf/orfig.cgi)在线软件预测PtJNK基因序列的开放阅读框(ORF)。利用ExPASy(http://cn.expasy.org/tools/pi_tool.html)、SMART (http://smart.embl-heidelberg.de)、SignalP 4.1 (http://www.cbs.dtu.dk/services/SignalP/)在线生物学分析软件对基因编码的氨基酸进行物理性质、结构域、跨膜结构域和信号肽的预测。使用DNA MAN 5.2.9软件对不同物种的氨基酸序列进行多重序列比对,并通过MEGA 6.0软件(Tamura et al, 2011)采用邻接法(Neighbor-Joining method) (Saitou et al, 1987)进行系统进化树的构建。
1.5 PtJNK基因组织表达分析将提取的总RNA用HiScript Ⅱ Q RT SuperMix for qPCR (+gDNA wiper) kit (南京诺维赞)进行反转录成cDNA,用于组织表达定量检测。根据PtJNK基因的全长序列,通过Primer Premier 5.0软件设计qRT-PCR特异性引物,内参基因选用β-actin(表 1)。采用10 µl qRT-PCR体系:SYBR Premix Ex Taq Ⅱ (2×) 5.0 µl,正/反向引物(10 µmol/L) 0.4 µl,ROX Reference Dye Ⅱ (50×) 0.2 µl,cDNA模板2.0 µl,灭菌水3.0 µl。反应程序:95℃ 30 s;95℃ 5 s,60℃ 34 s,40个循环;95℃ 15 s,60℃ 1.0 min,95℃ 15 s。采用2–∆∆Ct方法(Livak et al, 2001)对荧光定量结果进行分析,并通过SPSS 19.0软件进行显著性分析(P < 0.05)。
2 结果 2.1 PtJNK基因全长与序列结构特征利用RACE方法得到三疣梭子蟹JNK基因全长序列3240 bp,命名为PtJNK(GenBank登录号:MK28792)(图 1)。生物学软件分析显示,该基因包含5′非编码区668 bp,3′非编码区1192 bp,其开放阅读框(ORF)1380 bp,编码459个氨基酸,预测分子量为51.7 kDa,理论等电点为6.47。SMART、Signal 4.1在线软件分析显示,该氨基酸序列具有TPY磷酸化位点的S_TKC保守结构域(图 2),属于JNK基因家族典型结构特征,无信号肽及跨膜结构域。

|
图 1 三疣梭子蟹PtJNK基因cDNA全长及其编码的氨基酸序列 Fig.1 Nucleotide sequence and deduced amino acids sequence of PtJNK 起始密码子(ATG)和终止密码子(TAG)用方框标出;阴影部分为S_TKC保守结构域;TPY磷酸化位点用单下划线标出 Boxes: Start codon (ATG) and stop codon (TAG); Shadow: S_TKC Conservative domain; Underline: TPY phosphorylation |
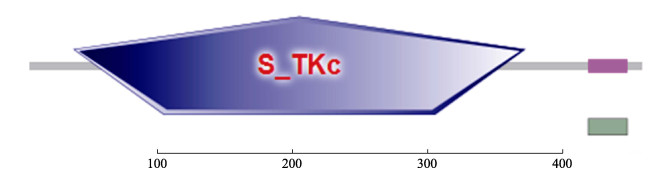
|
图 2 三疣梭子蟹PtJNK基因编码蛋白结构域位置 Fig.2 The protein domain architecture of PtJNK |
利用Blast在线软件对PtJNK氨基酸序列和其他物种的JNK氨基酸序列进行同源性比对,结果显示,PtJNK氨基酸序列与锯缘青蟹(Scylla paramamosain) SpJNK氨基酸序列同源性最高(91.7%),其次是中华绒螯蟹EsJNK(89.98%)、凡纳滨对虾PvJNK(88.52%)、日本对虾(Penaeus japonicas)PjJNK(87.90%)。利用DNA MAN对多个序列进行同源性比对发现(图 3),每个氨基酸序列都具有TPY磷酸化位点的S_TKC保守结构域结构。通过对多个氨基酸序列构建系统进化树发现(图 4),三疣梭子蟹与锯缘青蟹和中华绒螯蟹聚为一支,其次与凡纳滨对虾和日本对虾聚为一类。

|
图 3 三疣梭子蟹PtJNK氨基酸序列的多序列比对 Fig.3 The multiple sequence alignment of that PtJNKamino acid sequences 各物种名称及GenBank登录号:三疣梭子蟹MK28792;锯缘青蟹AYK28495.1;中华绒螯蟹AHG95993.1;凡纳滨对虾XP_027218684.1;日本对虾BAI87826.1;家蚕NP_001103396.1;果蝇AAB97094.1;乾木白蚁PNF21055.1;内华达古白蚁KDR18179.1;小鼠BAA85875.1;人NP_001310231.1 Name of each species and GenBank accession numbers: P. trituberculatus MK28792; S. paramamosain AYK28495.1; E. sinensis AHG95993.1; P. vannamei XP_027218684.1; P. japonicus BAI87826.1; B. mori NP_001103396.1; D. melanogaster AAB97094.1; C. secundus PNF21055.1; Z. nevadensis KDR18179.1; M. musculus BAA85875.1; H. sapiens NP_001310231.1 |
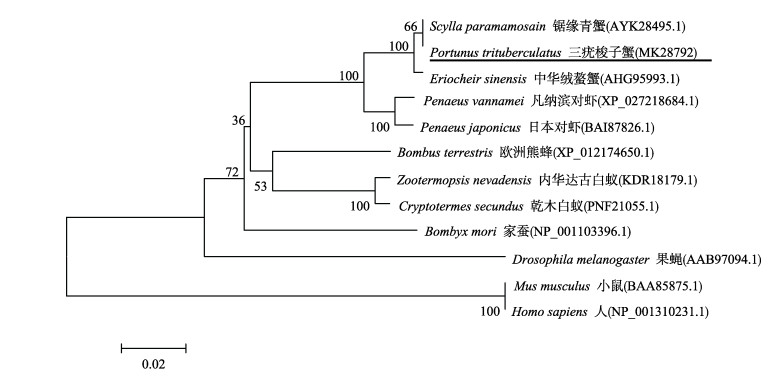
|
图 4 基于JNK氨基酸序列构建的不同物种的系统进化树 Fig.4 Phylogenetic tree of different species based on JNKamino acid sequences |
利用qRT- PCR技术对三疣梭子蟹不同组织的PtJNK mRNA进行相对表达定量检测,结果显示(图 5),PtJNK在各组织中都有表达,且表达存在显著差异(P < 0.05)。实验以肝胰腺作为对照,其中,胃和肌肉中的表达量最高(与肝胰腺的表达水平相比分别为3.98和3.78倍);其次在鳃的表达水平是肝胰腺的1.79倍;在心脏略低于肝胰腺的表达水平,在血细胞的相对表达量较低。因此,推测PtJNK可能在三疣梭子蟹中发挥不同的作用,其作用因组织类型的不同而不同。
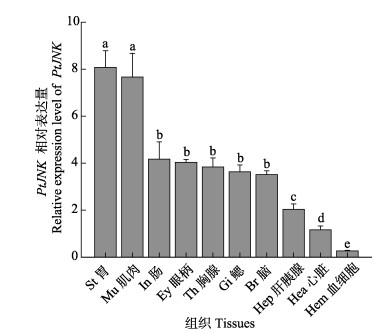
|
图 5 三疣梭子蟹PtJNK基因在不同组织中的表达 Fig.5 Relative expression characterization of PtJNK gene in the various tissues of P. trituberculatus 相同字母代表差异不显著(P > 0.05),不同字母代表差异显著(P < 0.05),下同 Same letters indicated no significantly different (P > 0.05), different letters indicated significantly different (P˂0.05). The same as below |
本研究利用qRT-PCR技术,研究在不同的病原刺激下,三疣梭子蟹血细胞、肝胰腺和鳃中JNK基因的表达情况(图 6)。在副溶血弧菌感染后,PtJNK基因在血细胞、鳃和肝胰腺3个组织中,与对照组相比基本呈现不同程度的下调趋势,且呈现先下降后上升再下降后趋于平衡的表达模式。在血细胞中,分别在12 h和24 h高于对照组表达量,达到最高表达水平,为对照组的1.79倍和1.54倍;在肝胰腺中,在12 h达到最高值,为对照组的0.63倍;在鳃中,在6 h达到最高表达量,为对照组的0.61倍,在48 h和72 h达到恒定水平,为对照组的0.56倍和0.59倍。
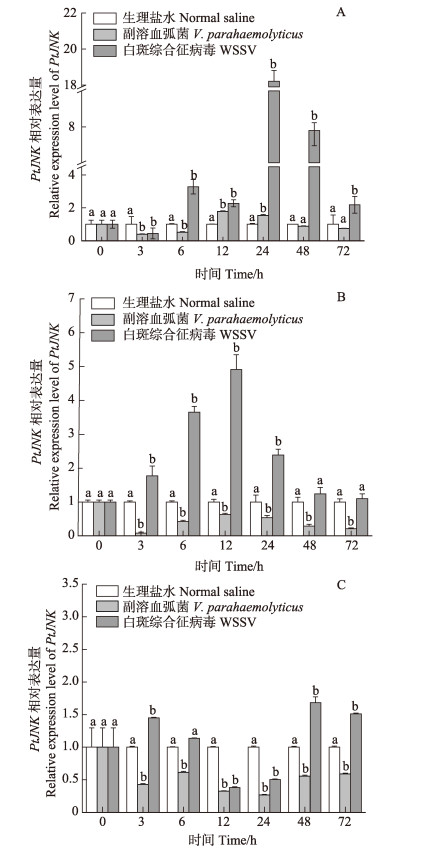
|
图 6 三疣梭子蟹在不同病原感染下PtJNK在血细胞(A)、肝胰腺(B)和鳃(C)中的表达模式 Fig.6 The expression of PtJNK in haemocytes (A), hepatopancreas(B), and gill(C) of P. trituberculatus after different pathogen infection 感染组间没有进行差异显著分析 No analysis was performed between infected groups |
在注射WSSV后,PtJNK基因在血细胞、肝胰腺和鳃3个组织中,相对对照组呈上调表达。在血细胞中呈先下降后上升再下降的表达模式,在24 h达到最大值,为对照组的18.21倍;在肝胰腺中,PtJNK基因的表达整体呈先上升后下降的表达趋势,在12 h表达量达到最大值,为对照组的4.91倍;在鳃中,PtJNK基因的表达整体呈先上升后下降再上升的表达趋势,其中,在12 h下调至最低水平,为对照组的0.38倍。
3 讨论为更加深入了解三疣梭子蟹JNK基因的分子特征,本研究首次获得PtJNK基因的全长序列,cDNA全长为3240 bp。经生物学软件分析,PtJNK基因含有TPY磷酸化位点的S_TKC保守结构域,是C-JUN氨基末端激酶(JNK)基因家族的典型结构域。氨基酸多重序列比对结果显示,PtJNK氨基酸序列与其他物种具有高度的保守性。系统进化树结果表明,无脊椎动物与脊椎动物有关JNK基因在进化上并没有十分密切的联系,而三疣梭子蟹PtJNK基因与锯缘青蟹、中华绒螯蟹聚为一支。综上所述,该序列确定为三疣梭子蟹JNK基因,且在进化上高度保守。
JNK基因可由各种环境应激激活,如细菌或病毒感染、氧化应激等。为了深入研究JNK基因在三疣梭子蟹中的功能,进行了病原感染实验,并利用qRT- PCR对PtJNK基因的组织表达模式进行了分析。结果显示,该基因在各检测组织(胃、肌肉、肠、眼柄、胸腺、鳃、脑、心脏、肝胰腺和血细胞)中均有表达,其中,在胃和肌肉中表达量最高。时恭芳(2017)在对斑节对虾(Penaeus monodon)的研究中发现,PmJNK在各组织中广泛表达,其中,在血淋巴、鰓和肠道中高表达;Sun等(2016)对虾夷扇贝(Patinopecten yessoensis)研究发现,JNK基因在肌肉中表达量最高。因此,推断PtJNK基因在三疣梭子蟹中可能参与多种生理表达,且因物种的不同其表达模式具有明显的差异。
在无脊椎动物中,血细胞(Wang et al, 2005; Bachère et al, 2004; Xiao et al, 2013)、肝胰腺(Diggles et al, 2000; Wang et al, 2012)被认为是主要的免疫器官,在宿主对外来病原体的免疫防御中发挥重要作用。为进一步研究PtJNK基因的功能,本研究对血细胞、鳃和肝胰腺3个组织进行了表达定量分析。研究发现,在注射副溶血弧菌后,PtJNK基因在血细胞、鳃和肝胰腺中的表达呈现一定程度的下调表达(P < 0.05),在3 h后,该基因的表达量呈先上升后下降的模式,而在对凡纳滨对虾(Li et al, 2015)和近江牡蛎(Crassostrea hongkongensis) (Qu et al, 2016)中研究发现,JNK基因呈上调表达,且在病原感染的过程中发挥着免疫调节作用,因此,推测副溶血弧菌导致三疣梭子蟹机体紊乱,引起PtJNK基因表达受到抑制,表明PtJNK基因参与了三疣梭子蟹免疫防御过程。WSSV感染后发现,在所观察的血细胞、肝胰腺和鳃中均呈现显著的上调表达(P < 0.05),分别在24 h、12 h和48 h达到最大值,为对照组的18.21倍、4.9倍和11.68倍,这与凡纳滨对虾的研究结果相似:Shi等(2012)的研究证明了该基因具有抑制WSSV复制的功能,Li等(2015)证明了JNK途径的激活(包括MKK7/ JNK/AP-1)可以增强抗菌肽(AMPs)的产生。另有研究发现,在病毒感染过程中,JNK信号通路参与病毒复制和调控特定病毒蛋白的表达(Sun et al, 2018; Li et al, 2015; Wei et al, 2015),而抗菌肽在机体免疫调节中具有重要的作用,这进一步证实了PtJNK基因在三疣梭子蟹免疫防御过程中起调节作用。
综上所述,本研究首次成功克隆得到三疣梭子蟹的PtJNK基因序列全长,并对其氨基酸序列进行了生物学分析,通过病原感染实验检测PtJNK基因在血细胞、肝胰腺和鳃中的相对表达量,初步证实了PtJNK基因在三疣梭子蟹感染病原的过程中发挥着重要的作用,为深入研究PtJNK基因的功能作用机制提供了理论参考。
Aoki H, Kang PM, Hampe J, et al. Direct activation of mitochondrial apoptosis machinery by c-Jun N-terminal kinase in adult cardiac myocytes. Journal of Biological Chemistry, 2002, 277(12): 10244-10250 DOI:10.1074/jbc.M112355200 |
Bachère E, Gueguen Y, Gonzalez M, et al. Insights into the anti-microbial defense of marine invertebrates: The penaeid shrimps and the oyster Crassostrea gigas. Immunological Reviews, 2004, 198(1): 149-168 |
Bond D, Foley E. A quantitative RNAi screen for JNK modifiers identifies Pvr as a novel regulator of Drosophila immune signaling. PLoS Pathogens, 2009, 5(11): 1000655 DOI:10.1371/journal.ppat.1000655 |
Davis RJ. Signal transduction by the JNK group of MAP kinases. Cell, 2000, 103(2): 239 DOI:10.1016/S0092-8674(00)00116-1 |
Delaney JR, Stoven S, Uvell H, et al. Cooperative control of Drosophila immune responses by the JNK and NF-kappaB signaling pathways. EMBO Journal, 2006, 25(13): 3068-3077 DOI:10.1038/sj.emboj.7601182 |
Dhanasekaran DN, Reddy EP. JNK signaling in apoptosis. Oncogene, 2008, 27(48): 6245-6251 DOI:10.1038/onc.2008.301 |
Diggles BK, Moss GA, Carson J, et al. Luminous vibriosis in rock lobster Jasus verreauxi (Decapoda: Palinuridae) phyllosoma larvae associated with infection by Vibrio harveyi. Diseases of Aquatic Organisms, 2000, 43(2): 127-137 |
Huang G, Shi LZ, Chi H. Regulation of JNK and p38 MAPK in the immune system: Signal integration, propagation and termination. Cytokine, 2009, 48(3): 161-169 DOI:10.1016/j.cyto.2009.08.002 |
Jones E, Dickman M, Whitmarsh A. Regulation of p73-mediated apoptosis by c-Jun N-terminal kinase. Biochemical Journal, 2007, 405(3): 617-623 |
Kyriakis JM, Banerjee P, Nikolakaki E, et al. The stress- activated protein kinase subfamily of c-Jun kinases. Nature, 1994, 369(6476): 156-160 DOI:10.1038/369156a0 |
Li C, Li H, Wang S, et al. The c-Fos and c-Jun from Litopenaeus vannamei play opposite roles in Vibrio parahaemolyticus and white spot syndrome virus infection. Developmental and Comparative Immunology, 2015, 52(1): 26-36 DOI:10.1016/j.dci.2015.04.009 |
Li L. Common diseases and their control of swimming crab, Portunus trituberculatus. Fisheries Science and Technology Information, 2005, 32(6): 269-271 [李卢. 三疣梭子蟹的常见病及其防治. 水产科技情报, 2005, 32(6): 269-271] |
Lin A. Activation of the JNK signaling pathway: Breaking the brake on apoptosis. Bioessays News and Reviews in Molecular Cellular and Developmental Biology, 2003, 25(1): 17-24 DOI:10.1002/bies.10204 |
Livak KJ, Schmittgen TD. Analysis of relative gene expression data using real-time quantitative PCR and the 2(-Delta Delta C(T) method. Methods, 2001, 25(4): 402-408 |
Minden A, Karin M. Regulation and function of the JNK subgroup of MAP kinases. Letters in Spatial and Resource Sciences, 2008, 1333(2): 85-104 |
Qu F, Xiang Z, Xiao S, et al. c-Jun N-terminal kinase (JNK) is involved in immune defense against bacterial infection in Crassostrea hongkongensis. Developmental and Comparative Immunology, 2016, 67: 77-85 |
Ren HB, Li YB, Zhang XR, et al. Molecular cloning and sequence analysis of Scygonadin from Portunus trituberculatus. Journal of Biology, 2018, 35(4): 21-24 [任海波, 李燕波, 张肖荣, 等. 三疣梭子蟹抗菌肽Scygonadin基因的克隆与序列分析. 生物学杂志, 2018, 35(4): 21-24] |
Saitou N, Nei M. The neighbor-joining method: A new method for reconstructing phylogenetic trees. Molecular Biology and Evolution, 1987, 4(4): 406-425 |
Shi GF. The cloning and function research of the genes JNK, C-JUN and ATF-2 in the JNK signaling pathway from shrimp, Penaeus monodon. Masterxs Thesis of Shanghai Ocean University, 2017 [时恭芳.斑节对虾JNK信号通路中的JNK、C-JUN和ATF-2基因的克隆与功能研究.上海海洋大学硕士研究生学位论文, 2017]
|
Shi H, Yan X, Ruan L, et al. A novel JNK from Litopenaeus vannamei involved in white spot syndrome virus infection. Developmental and Comparative Immunology, 2012, 37(3-4): 421-428 DOI:10.1016/j.dci.2012.03.002 |
Sluss HK, Goberdhan DC, Davis RJ, et al. A JNK signal transduction pathway that mediates morphogenesis and an immune response in Drosophila. Genes and Development, 1996, 10(21): 2745-2758 DOI:10.1101/gad.10.21.2745 |
Sun J, Li Y, Li M, et al. A novel JNK is involved in immune response by regulating IL expression in oyster, Crassostrea gigas. Fish and Shellfish Immunology, 2018, 79: 93-101 DOI:10.1016/j.fsi.2018.05.017 |
Sun Y, Zhang L, Zhang M, et al. Characterization of three mitogen-activated protein kinases (MAPK) genes reveals involvement of ERK and JNK, not p38 in defense against bacterial infection in Yesso scallop Patinopecten yessoensis. Fish and Shellfish Immunology, 2016, 54: 507-515 DOI:10.1016/j.fsi.2016.04.139 |
Tamura K, Peterson D, Peterson N, et al. MEGA5: Molecular evolutionary genetics analysis using maximum likelihood, evolutionary distance, and maximum parsimony methods. Molecular Biology and Evolution, 2011, 28(10): 2731-2739 DOI:10.1093/molbev/msr121 |
Wang PH, Liang JP, Gu ZH, et al. Molecular cloning, characterization and expression analysis of two novel Tolls (LvToll2 and LvToll3) and three putative Sp tzle-like Toll ligands (LvSpz1-3) from Litopenaeus vannamei. Developmental and Comparative Immunology, 2012, 36(2): 359-371 DOI:10.1016/j.dci.2011.07.007 |
Wang Y, Puscheck EE, Lewis JJ, et al. Increases in phosphorylation of SAPK/JNK and p38MAPK correlate negatively with mouse embryo development after culture in different media. Fertility and Sterility, 2005, 83(1): 1144-1154 |
Wei S, Huang Y, Huang X, et al. Characterization of c-Jun from orange-spotted grouper, Epinephelus coioides involved in SGIV infection. Fish and Shellfish Immunology, 2015, 1(43): 230-240 |
Xiao YM, Zhou YH, Xiong Z, et al. Involvement of JNK in the embryonic development and organogenesis in zebrafish. Marine Biotechnology, 2013, 15(6): 716-725 DOI:10.1007/s10126-013-9520-5 |
Yan BL, Liang LG, Zhang XJ. Prevention and cure of fish disease proceedings on main diseases of swimming crab, Portunus trituberculatus. Fisheries Science and Technology Information, 2010, 37(1): 29-33 [阎斌伦, 梁利国, 张晓君. 三疣梭子蟹主要病害研究进展. 水产科技情报, 2010, 37(1): 29-33] |
Zhang J, Lü JJ, Liu P, et al. Cloning of Toll4 in Portunus trituberculatus and its expression in responding to pathogenic infection and low salinity stress. Progress in Fishery Sciences, 2018, 39(2): 146-155 [张杰, 吕建建, 刘萍, 等. 三疣梭子蟹Toll4基因克隆及其在病原和低盐胁迫中的表达特征分析. 渔业科学进展, 2018, 39(2): 146-155] |
Zhang W, Liu HT. MAPK signal pathways in the regulation of cell proliferation in mammalian cells. Cell Research, 2002, 12(1): 9-18 |
Zhou JF, Li XC, Wang JY, et al. Analysis of major infectious diseases and their causative agents of Chinese sea crab. Marine Sciences, 2014, 38(6): 102-106 [周俊芳, 李新苍, 王江勇, 等. 中国海水蟹主要流行性疾病及其病原分析. 海洋科学, 2014, 38(6): 102-106] |
Zhu YT, Zhang X, Wang SC, et al. Antimicrobial functions of EsLecH, a C-type lectin, via JNK pathway in the Chinese mitten crab, Eriocheir sinensis. Developmental and Comparative Immunology, 2016, 61: 225-235 DOI:10.1016/j.dci.2016.04.007 |



