2. 中国水产科学研究院黄海水产研究所 农业农村部海洋渔业可持续发展重点实验室 青岛 266071;
3. 青岛海洋科学与技术试点国家实验室 海洋渔业科学与食物产出过程功能实验室 青岛 266071;
4. 上海海洋大学水产与生命学院 上海 201306
Glucose Metabolism of Marsupenaeus japonicas
2. Yellow Sea Fisheries Research Institue, Chinese Academy of Fishery Sciences, Key Laboratory of Sustainable Development of Marine Fisheries, Ministry of Agriculture and Rural Affairs, Qingdao 266071;
3. Laboratory for Marine Fisheries Science and Food Production Processes, Pilot National Laboratory for Marine Science and Technology (Qingdao), Qingdao 266071;
4. College of Fisheries and Life Science, Shanghai Ocean University, Shanghai 201306
日本囊对虾(Marsupenaeus japonicas)原称日本对虾,其肉质鲜嫩,具有耐低温、耐干燥、生长速度快、价格远高于其他经济虾类等优点,现已成为许多沿海地区的重要养殖品种(王克行, 1997)。目前,日本囊对虾主要以池塘养殖为主,养殖密度偏低,同时,又受底质选择(徐涵等, 2015)、病害频发(韩琳等, 2018)、同类相残(陈学雷等, 2003)等因素的影响,养殖难度加大。日本囊对虾近2~3年总体产量不断增加(袁晓初等, 2016; 徐乐俊等, 2018),但仍然满足不了当前市场的需求,供需矛盾上升,急需探寻一种新的养殖模式来解决此问题。对虾工厂化养殖始于20世纪末,在凡纳滨对虾(Litopenaeus vannamei)养殖中应用较为成熟,但因日本囊对虾有底质选择、同类相残、昼伏夜出的生物学特性,难以直接借鉴凡纳滨对虾工厂化养殖的经验(李玉全等, 2013)。
光作为重要环境因子,直接或间接影响水生动物的生长、摄食、存活和繁殖等(周显青等, 2000)。周期性的光强变化和光色波动都会影响凡纳滨对虾的生长(Guo et al, 2012、2013),不同的光照周期也会影响刺龙虾(Sagmariasus verreauxi)的幼体变态发育(Fitzgibbon et al, 2012);在室内条件下,LED灯作为光源可以提高凡纳滨对虾的成活率和产量(Fleckenstein et al, 2019);王馨等(2014)研究不同光照强度对三疣梭子蟹(Portunus trituberculatus)呼吸代谢的影响,表明三疣梭子蟹工厂化养殖的适宜光照强度为1500 lx;刘伟等(2011)研究表明,不同光色对中国明对虾(Fenneropenaeus chinensis)稚虾耗氧率昼夜变化节律影响显著,蓝色光下,中国明对虾代谢耗能较高、存活率较低;同时,光也会通过光照强度和光照周期的变化影响甲壳动物的蜕皮抑制激素(MIH)的分泌,进而影响其蜕皮过程(李旭光等, 2014)。在大多数有眼柄的甲壳动物中存在X-器窦腺复合体,该器官合成和分泌高血糖激素家族,包括高血糖激素(CHH)、MIH、性腺抑制激素(GIH)和大鄂器抑制激素(MOIH)。它们协同调控甲壳动物的生长、繁殖、蜕壳等生理生化过程,其中,蜕皮主要受眼柄中MIH和Y器中蜕皮激素(EH)的调控(杨济芬等, 2009; 亓一舟等, 2010)。当甲壳动物受到外界压力时,多种神经递质[5-羟色胺(5-HT)]等会促进X-器窦腺复合体中的高血糖激素家族分泌,MIH阻碍EH的分泌,高血糖激素也参与蜕皮的调控,在这个过程中起抑制作用,同时,高血糖激素调节血糖水平(de Kleijn et al, 1995; Fanjul-Moles, 2006),调控肝胰腺中的糖原代谢,维持各个组织与器官的能量供应;而在糖原代谢过程中,存在关键性的酶来调控此反应的进行,糖原磷酸化酶(GP)是糖原分解中重要的限速酶,糖原合酶(GS)控制着糖原生成的速度(Nagai et al, 2011)。日本囊对虾有昼伏夜出的生活习性,所以,对光照周期也有一定的要求,此前关于光照对日本囊对虾生长的研究已有报道,但仅停留在存活率、生长等表观指标方面(周志华等, 1999),罕见其有关生理影响机制方面的报道。本研究以日本囊对虾为对象,在室内条件下,探究不同光照时间对日本囊对虾生长、蜕皮和糖代谢的影响,以期为日本囊对虾工厂化养殖提供参考数据。
1 材料与方法 1.1 实验材料实验于2018年7月7日~9月5日在山东潍坊海丰水产养殖有限责任公司进行,历时60 d。日本囊对虾苗购于山东日照海辰水产有限公司,经过约15 d的暂养后用于实验。暂养期间,水体溶解氧(DO) > 5 mg/L,日换水量为总水量的20%~30%,每日投喂4次(07:00、12:00、17:00、22:00)冰鲜大卤虫(Artemia salina)。白天和晚上投喂比例为4:6;投喂量占虾总体重的15%~20%。实验用沙购于市场,经筛网筛选后,得到粒径不超过0.5 mm的细沙,并经ClO2溶液消毒处理,清水冲洗,晾干后备用。实验对象初始体长为(1.930±0.217) cm,初始体重为(0.064±0.020) g。
1.2 实验设计本实验设置全黑暗(D),光照:黑暗=10L:14D,光照:黑暗=14L:10D,全光照(L) 4个不同的实验组,所有实验组均设置3个平行,所用光源为白炽灯,光照强度为200 lx。在体积为200 L的白色PVC桶中进行实验,内铺设厚度为10 cm的细沙,注水140 L,每桶放30尾日本囊对虾,在桶的最上层固定网目为10目的纱网,以防止日本囊对虾跳出。
1.3 实验管理实验期间,日投饵量约为日本囊对虾体重的10%~15%,分别于08:00、17:00进行投喂,上午:傍晚投喂比例为3:7;每日07:00用虹吸管换底层水20%~ 30%,所用海水为自然海水,水温为26.1℃~31.5℃,盐度为30.69~33.46,pH为7.94~8.22。实验期间,保持连续充气,使水体DO含量≥5mg/L,发现死虾及时捞出。
1.4 样品收集和指标测定实验前随机取30尾日本囊对虾测量体重。实验期间,每隔30 d从各实验组随机选取6尾日本囊对虾(蜕壳间期),分别取血清、肝胰腺,所有操作均在冰上进行。测血清中5-HT、CHH、MIH、EH的浓度;测肝胰腺中GS、GP的酶活,上述指标均由上海酶联生物科技有限公司提供的试剂盒测定,所有操作按说明书上的步骤进行。血清是经血液与抗凝剂(柠檬酸酸三钠7.49 g/L、NaCl 19.6 g/L、葡萄糖22.8 g/L、乙二胺四乙酸二钠3.3 g/L、pH为7.5)体积1:1混合后,4℃,3500 r/min离心10 min获得。每日统计不同光照周期组的日本囊对虾蜕壳数;实验结束后,统计各组存活个数,并测量其体重。
1.5 数据计算与统计分析实验结束后,日本囊对虾的成活率(Survival rate, SR, %)、体重特定生长率(Specific growth rate, SGR, %/d)和蜕壳率(Molting frequency rate, MF, %/d)分别按下列公式计算:
| $ {\rm SR}\left(\% \right) = \left({{N_1}-{N_2}} \right)/{N_1} \times 100 $ |
| $ {\rm SGR}\left({\% /{\rm d}} \right) = \left({\ln {W_2}-\ln {W_1}} \right)/T \times 100 $ |
| $ {\rm MF}\left({\% /{\rm d}} \right) = \left({{N_m}/{N_s}} \right)/T $ |
式中,N1和N2为实验开始时日本囊对虾个数和结束时死亡对虾的个数,W2和W1为结束和初始时对虾的湿重(g);T为实验持续的时间(d);Nm为实验期间蜕壳次数;Ns为每桶养虾数。
采用SPSS 25.0软件进行数据分析,利用单因素方差(One-way ANOVA)和多重比较检验分析不同光照组日本囊对虾生长、神经递质5-HT、各激素浓度和糖代谢酶活性的差异,P < 0.05为显著水平。采用Origin 2018软件绘制图表。
2 结果 2.1 光照周期对日本囊对虾存活、生长、蜕皮的影响不同光照周期对日本囊对虾存活、生长、蜕皮的影响见表 1。从表 1可以看出,经过不同的光照时间,日本囊对虾的存活情况受到不同程度的影响。实验进行到49 d时,L组日本囊对虾已全部死亡;实验结束时,D组SR最高,为(60.000±2.722)%,14L:10D组和10L:14D组SR差异不显著(P > 0.05),但随着光照时间的增加,SR显著下降(P < 0.05)。
|
|
表 1 不同光照周期对日本囊对虾存活、生长、蜕皮的影响 Tab.1 Effects of different photoperiod on survival, growth and molting of M. japonicas |
光照周期显著影响日本囊对虾的生长(表 1)。L组实验结束时,日本囊对虾全部死亡,其SGR没有数据。D组的SGR最高,为(6.966±0.686)%/d,显著高于14L:10D和10L:14D组,10L:14D和14L:10D组相比差异不显著(P > 0.05)。
不同光照周期对日本囊对虾MF有显著影响。D组的MF显著高于14L:10D和10L:14D组,为(4.667± 0.363)%/d (P < 0.05),10L:14D和14L:10D组相比差异不显著(P > 0.05)。
2.2 光照周期对日本囊对虾 5-HT、CHH、MIN 和 EH 浓度的影响实验结束时,L组日本囊对虾已全部死亡,无法取样,相关指标无法检测,因此,60 d时只能进行前3个实验组的比较。
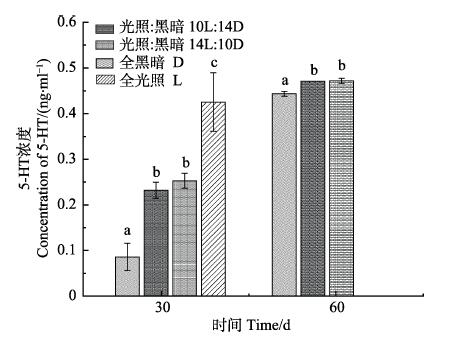
不同光照周期对日本囊对虾5-HT浓度的影响见图 1。从图 1可以看出,30 d时,随着光照时间的延长,对虾血清中的5-HT浓度不断提高,D组的5-HT浓度显著低于其他3个实验组(P < 0.05),为(0.086± 0.030) ng/ml;10L:14D和14L:10D组的5-HT浓度显著低于L组(P < 0.05),但10L:14D和14L:10D组间相比差异不显著(P > 0.05)。随着实验的进行,各个实验组的5-HT浓度均有不同程度的增加;60 d时,D组的5-HT浓度显著低于10L:14D和14L:10D组,为(0.444±0.005) ng/ml (P < 0.05);但10L:14D和14L:10D组间相比差异不显著(P > 0.05)。
|
图 1 不同光照周期对日本囊对虾5-HT浓度的影响 Fig.1 Effects of different photoperiod on the concentrations of 5-HT in M. japonicas 同一时间不同字母表示差异显著(P < 0.05),下同 Different letters indicate significant differences at the same time, the same as below |
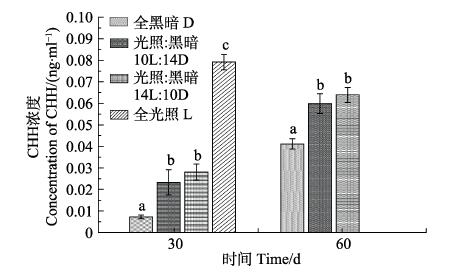
不同光照周期对CHH浓度的影响见图 2。从图 2可以看出,随着实验的进行,不同处理组的CHH浓度不断提高。30 d时,随着光照时间的延长,各实验组的CHH浓度不断升高,D组的CHH浓度显著低于10L:14D、14L:10D和L组(P < 0.05),为(0.007± 0.001) ng/ml;10L:14D和14L:10D组显著低于L组(P < 0.05),但10L:14D和14L:10D组相比差异不显著(P > 0.05)。60 d时,D组的CHH浓度显著低于10L:14D和14L:10D组(P < 0.05),为(0.041±0.002) ng/ml,10L:14D和14L:10D组相比无显著差异。
|
图 2 不同光照周期对日本囊对虾CHH浓度的影响 Fig.2 Effects of different photoperiod on the concentrations of CHH in M. japonicas |
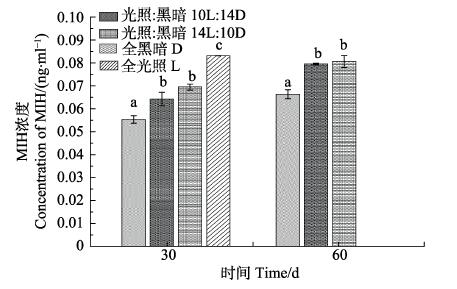
不同光照周期对MIH浓度的影响见图 3。从图 3可以看出,实验进行30、60 d时,随着光照周期的增强,日本囊对虾血清中的MIH浓度不断升高。30 d时,D组的MIH浓度显著低于其余3个实验组(P < 0.05),为(0.055±0.002) ng/ml,10L:14D和14L:10D组间无显著差异(P > 0.05),但这2个实验组显著低于L组(P < 0.05)。60 d时,D组显著低于10L:14D组和14L:10D组,为(0.066±0.002) ng/ml;10L:14D和14L:10D组间差异不显著(P > 0.05)。
|
图 3 不同光照周期对日本囊对虾MIH浓度的影响 Fig.3 Effects of different photoperiod on the concentrations of MIH in M. japonicas |
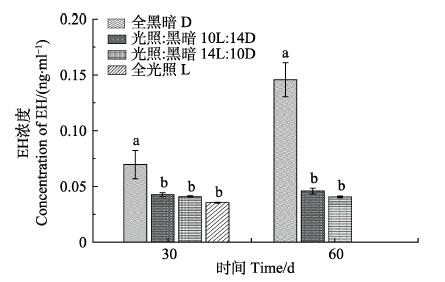
不同光照周期对EH浓度的影响见图 4。从图 4可以看出,30、60 d时,随着光照时间的延长,日本囊对虾血清中的EH浓度不断降低。其中,30 d时,D组的EH浓度显著高于其余3个实验组(P < 0.05),为(0.070±0.012) ng/ml,剩余3个实验组间无显著差异,但L组的EH浓度是4个实验组中最低的。60 d时,D组的EH浓度显著高于10L:14D和14L:10D组(P < 0.05),为(0.146±0.015) ng/ml;10L:14D和14L:10D组相比无显著差异(P > 0.05)。
|
图 4 不同光照周期对日本囊对虾EH浓度的影响 Fig.4 Effects of different photoperiod on the concentrations of EH in M. japonicas |
不同光照周期对GP活性的影响见图 5。从图 5可以看出,实验进行30、60 d时,随着光照时间的延长,对虾肝胰腺中的GP活性不断升高。30 d时,D组GP活性显著低于其余3个实验组(P < 0.05),为(0.088±0.009)U/ml,10L:14D和14L:10D组相比无显著差异,但这2个组显著低于L组(P < 0.05)。60 d时,D组显著低于10L:14D和14L:10D组,为(1.173± 0.400) U/ml;10L:14D和14L:10D组相比差异不显著(P > 0.05)。

|
图 5 不同光照周期对日本囊对虾GP活性的影响 Fig.5 Effects of different photoperiod on the activity of GP in M. japonicas |
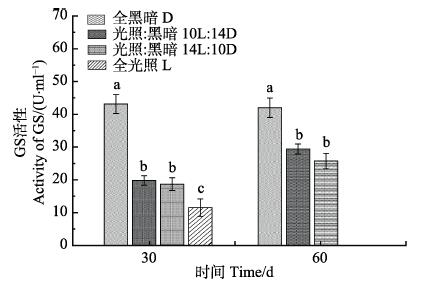
不同光照周期对GS活性的影响见图 6。从图 6可以看出,30、60 d时,随着光照时间的延长,日本囊对虾肝胰腺中的GS活性不断降低。其中,30 d时,D组的GP显著高于其余3个组(P < 0.05),为(43.155± 2.844) U/ml,10L:14D和14L:10D组相比无显著差异,但这2个实验组显著高于L组(P < 0.05)。60 d时,D组的GP显著高于10L:14D和14L:10D组,为(41.997±2.942) U/ml;10L:14D组和14L:10D组相比差异不显著(P > 0.05)。
|
图 6 不同光照周期对日本囊对虾GS活性的影响 Fig.6 Effects of different photoperiod on the activity of GS in M. japonicas |
许多研究表明,光照周期对甲壳动物的存活和生长有影响,但因种而异(王芳等, 2004; Baloi et al, 2013; Pati et al, 2015; 俞震颉等, 2016)。王芳等(2005)研究表明,14L:10D和18L:6D光周期不影响中国对虾的生长;周志华等(1999)研究表明,全黑暗状态下,日本囊对虾的存活率和生长率最高;Pati等(2015)研究表明,黑暗状态下,斑节对虾(Penaeus monodon)的生长速度最快;Andrés等(2010)研究认为,远海梭子蟹(Portunus pelagicus)最适宜生长的光周期为18L:6D。本研究结果显示,全黑暗状态下,日本囊对虾的SR、SGR、MF最高,10L:14D和14L:10D组相比差异不显著;与周志华等(1999)、Pati等(2015)的研究结果基本一致,与>Andrés等(2010)的研究结果有所不同。可见,不同物种间最适宜生长的光照周期是有所差异的。
3.2 不同光照周期对甲壳动物蜕皮的影响甲壳动物的生长与蜕皮主要受不同神经激素的调控(Chen et al, 2003),而生物胺主要调节这些激素的合成和释放(Richardson et al, 1991)。5-HT作为生物胺的一种,是存在甲壳动物神经系统中的一种重要神经递质,间接调节各种生理过程,包括新陈代谢、繁殖和甲壳动物的蜕皮等(Fingerman et al, 1994)。当受到外界环境胁迫时,甲壳动物会释放神经递质(5-HT等)促进MIH的释放,从而对蜕皮进行调控,同时,甲壳动物蜕皮也受Y器官分泌EH的调节,这2种激素有拮抗的作用(de Kleijn et al, 1995; Fanjul-Moles, 2006)。Aiken(1969)研究表明,长时间光照会抑制甲壳动物的MIH合成与释放,从而缩短蜕皮周期时间,短时间光照则效果相反。而徐建荣等(2006)则认为,光照对甲壳动物蜕皮的影响因其不同发育阶段的变化而变化,长时间光照会影响中华绒毛蟹(Eriocheir sinensis)Ⅰ~Ⅳ期幼蟹的蜕壳生长,而当大眼幼体变态发育到Ⅰ期仔蟹后,对光照的适应性也由趋光性转为避光性,主动选择水草以及掩蔽物等弱光区域进行蜕皮。本研究表明,随着光照时间的延长,日本囊对虾体内的5-HT浓度不断升高,MIH浓度也随光照时间的增加而不断升高,EH浓度有下降的趋势,最终不同组的MF也呈显著下降的趋势。D组的5-HT、MIH浓度显著低于有光照组(P < 0.05),EH浓度显著高于有光照组,但有光照组间差异不显著;D组的MF显著高于10L:14D和14L:10D组(P < 0.05),10L:14D和14L:10D组之间差异不显著。这表明在黑暗状态下,日本囊对虾受到的胁迫程度最小,最适宜生存,而全光照下,日本囊对虾受到的胁迫程度最大,最不适宜其生存。本研究中,EH浓度的变化趋势与MF有所不同,推测光照时间达到一定时长后,可能不会对蜕皮激素的分泌产生促进作用,但同时对其产生作用的光照时长范围还未确定,有待进一步研究。
3.3 不同光照周期对甲壳动物糖代谢的影响当受到外界环境胁迫时,甲壳动物会释放神经递质(5-HT等)促进CHH的释放,CHH作用于肝胰腺,参与糖原代谢,从而调节血糖水平(杨济芬等, 2009; Nagai et al, 2011; Fossat et al, 2014)。在糖原代谢过程中,存在2种调节糖原的合成和分解至关重要的酶,分别为GS和GP。本研究中,随着光照时间的延长,5-HT浓度不断提高,CHH激素也不断增加,GP活性不断上升,而GS活性不断降低。第30天时,D组的5-HT、CHH浓度和GP活性显著低于光照组(P < 0.05),10L:14D和14L:10D组间差异不显著,但是低于L组(P < 0.05);D组GS活性显著高于光照组(P < 0.05),10L:14D和14L:10D组间差异不显著,但显著高于L组(P < 0.05)。第60天时,日本囊对虾5-HT、CHH、GP、GS含量呈现与第30天相同的趋势。这表明在全黑暗状态下,糖原分解代谢水平最低,有利于糖原积累,进而促进对虾的生长。有研究表明,在凡纳滨对虾体内注射多巴胺(DA)、5-HT后,血淋巴酚氧化酶活力明显升高,溶菌和抗菌活力显著下降,而且DA比5-HT对免疫指标的影响更显著(胡发文等, 2007)。生物胺作为一种神经内分泌信号,引发甲壳动物产生不同的免疫应激适应过程,导致机体免疫防御能力下降。本研究结果表明,5-HT浓度随光照时间的延长而增加,从侧面也说明,光照时间越长,日本囊对虾机体免疫能力越低,其SR也越低。综上所述,日本囊对虾最适宜生长的环境为黑暗状态。
Aiken DE. Photoperiod, endocrinology and the crustacean moult cycle. Science, 1969, 164: 149-155 |
Andrés M, Rotllant G, Zeng CS. Survival, development and growth of larvae of the blue swimmer crab, Portunus pelagicus, cultured under different photoperiod conditions. Aquaculture, 2010, 300(1-4): 218-222 |
Baloi M, Arantes R, Schveitzer R, et al. Performance of Pacific white shrimp Litopenaeus vannamei raised in biofloc systems with varying levels of light exposure. Aquacultural Engineering, 2013, 52: 39-44 DOI:10.1016/j.aquaeng.2012.07.003 |
Chen XL, Lin QW, Li SJ, et al. Observations and studies on the cannibalism among post larvae of kuruma prawn, Penaeus japonicus. Journal of Xiamen University (Natural Science), 2003, 42(3): 358-362 |
陈学雷, 林琼武, 李少菁, 等. 日本对虾仔虾相残的实验研究. 厦门大学学报(自然科学版), 2003, 42(3): 358-362 |
Chen YN, Fan HF, Hsieh SL, et al. Physiological involvement of DA in ovarian development of the freshwater giant prawn, Macrobrachium rosenbergii. Aquaculture, 2003, 228(1): 383-395 |
de Kleijn DP, van Herp F. Molecular biology of neurohormone precursors in the eyestalk of crustacea. Comp arative Biochemistry and Physiology B: Biochemistry and Molecular Biology, 1995, 112(4): 573-579 DOI:10.1016/0305-0491(95)00126-3 |
Fanjul-Moles ML. Biochemical and functional aspects of crustacean hyperglycemic hormone in decapod crustaceans: Review and update. Comparative Biochemistry and Physiology Part C: Toxicology and Pharmacology, 2006, 142(3-4): 390-400 DOI:10.1016/j.cbpc.2005.11.021 |
Fingerman M, Nagabhushanam R, Rachakonda S, et al. Biogenic amines in crustaceans: identification, localization, and roles. Journal of Crustacean Biology, 1994, 14(3): 413-437 DOI:10.1163/193724094X00010 |
Fitzgibbon QP, Battaglene SC. Effect of photoperiod on the culture of early-stage phyllosoma and metamorphosis of spiny lobster (Sagmariasus verreauxi). Aquaculture, 2012, 368-369: 48-54 DOI:10.1016/j.aquaculture.2012.09.018 |
Fleckenstein LJ, Tierney TW, Fisk JC, et al. Effects of supplemental LED lighting on water quality and Pacific white shrimp (Litopenaeus vannamei) performance in intensive recirculating systems. Aquaculture, 2019, 504: 219-226 DOI:10.1016/j.aquaculture.2019.01.066 |
Fossat P, Bacque-Cazenave J, De Deurwaerdere P, et al. Anxiety-like behavior in crayfish is controlled by serotonin. Science, 2014, 344(6189): 1293-1297 DOI:10.1126/science.1248811 |
Guo B, Wang F, Li Y, et al. Effect of periodic light intensity change on the molting frequency and growth of Litopenaeus vannamei. Aquaculture, 2013, 396-399: 66-70 DOI:10.1016/j.aquaculture.2013.02.033 |
Guo B, Mu YC, Wang F, et al. Effect of periodic light color change on the molting frequency and growth of Litopenaeus vannamei. Aquaculture, 2012, 362-363: 67-71 DOI:10.1016/j.aquaculture.2012.07.034 |
Han L, Wang XH, Yang B, et al. Analysis of pathogen in an outbreak death of Marsupenaeus japonicus. Journal of Fisheries of China, 2018, 42(3): 431-441 |
韩琳, 王秀华, 杨冰, 等. 一例日本囊对虾暴发性死亡的病原分析. 水产学报, 2018, 42(3): 431-441 |
Hu FW, Pan LQ, Yang HZ. ffects of injecting biogenic amines on immune parameters of white shrimp Litopenaeus vannamei. 热带海洋学报, 2007, 26(5): 64-68 |
胡发文, 潘鲁青, 杨慧赞. 注射生物胺对凡纳滨对虾免疫指标的影响. 热带海洋学报, 2007, 26(5): 64-68 |
Li XG, Zhou G, Gu XH. Review of aquatic crustaceans molting and its influencing factors. Chinese Journal of Zoology, 2014, 49(2): 294-302 |
李旭光, 周刚, 谷孝鸿. 水生甲壳类蜕皮发生过程及其影响因素的研究与进展. 动物学杂志, 2014, 49(2): 294-302 |
Li YQ, Wang RJ, Jiang LX. Effects of density-stress on water quality and growth of Marsupenaeus japonicus. Marine Sciences, 2013, 37(10): 53-57 |
李玉全, 王仁杰, 姜令绪. 密度胁迫对日本囊对虾生长和水环境的影响. 海洋科学, 2013, 37(10): 53-57 |
Liu W, Wang F, Zhong DS, et al. The effect of light colour on the diel rhythm of oxygen consumption rate in juvenile Chinese shrimp, Fenneropenaeus Chinensis. Transactions of Oceanology and Limnology, 2011(3): 27-31 |
刘伟, 王芳, 钟大森, 等. 光色对中国明对虾(Fenneropenaeus chinensis)稚虾耗氧率昼夜变化节律的影响. 海洋湖沼通报, 2011(3): 27-31 |
Nagai C, Nagata S, Nagasawa H. Effects of crustacean hyperglycemic hormone (CHH) on the transcript expression of carbohydrate metabolism-related enzyme genes in the kuruma prawn, Marsupenaeus japonicus. General and Comparative Endocrinology, 2011, 172(2): 293-304 |
Pati S, Chatterji A, BP D. A study on the growth of juveniles of tiger prawn, Penaeus monodon (Fabricius) under different photoperiods. Journal of Aquaculture Research and Development, 2015, 6(12): 385 |
Qi YZ, Zhu DF, Yang JF, et al. Cellular mechanism of molt- inhibiting hormone action in the crustacean. Chinese Journal of Zoology, 2010, 45(2): 165-170 |
亓一舟, 朱冬发, 杨济芬, 等. 甲壳动物蜕皮抑制激素调控机制的研究进展. 动物学杂志, 2010, 45(2): 165-170 |
Richardson HG, Deecaraman M, Fingerman M. The effect of biogenic amines on ovarian development in the fiddler crab, Uca pugilator. Comparative Biochemistry and Physiology Part C: Comparative Pharmacology, 1991, C99: 53-56 |
Wang F, Dong SL, Dong SS, et al. Effects of photoperiod on the molting and growth of juvenile Chinese shrimp Fenneropenaeus chinensis. Journal of Fishery Sciences of China, 2004, 11(4): 354-359 |
王芳, 董双林, 董少帅, 等. 光照周期对中国对虾稚虾蜕皮和生长的影响. 中国水产科学, 2004, 11(4): 354-359 |
Wang F, Zhang JD, Dong SL, et al. The effects of light intensity and photoperiod on the growth of juvenile Fenneropenaeus chinensis. Periodical of Ocean University of China(Natural Science), 2005, 35(5): 768-772 |
王芳, 张建东, 董双林, 等. 光照强度和光照周期对中国明对虾稚虾生长的影响. 中国海洋大学学报(自然科学版), 2005, 35(5): 768-772 |
Wang KX. Shrimp and crab aquaculture. Beijing: China Agriculture Press, 1997: 218-219
|
王克行. 虾蟹类增养殖学. 北京: 中国农业出版社, 1997: 218-219
|
Wang X, Wang F, Lu YL, et al. Effects of light intensity on the respiratory metabolism of swimming crab (Portunus trituberculatus). Journal of Fisheries of China, 2014, 38(2): 237-243 |
王馨, 王芳, 路允良, 等. 光照强度对三疣梭子蟹呼吸代谢的影响. 水产学报, 2014, 38(2): 237-243 |
Xu H, Xiong DL, Wu YL, et al. Effects of breeding density and substratum types on growth and survival of Marsupenaeus japonicus. Hubei Agricultural Sciences, 2015, 54(4): 923-925 |
徐涵, 熊慧, 吴亚林, 等. 养殖密度、底质类型对日本囊对虾生长、存活的影响. 湖北农业科学, 2015, 54(4): 923-925 |
Xu JR, Shen SD, Zhang JM, et al. Influence of environment on molting and growth of Chinese mitten crab (Eriocheir sinensis) Megalopa. Fisheries Science, 2006(10): 505-508 |
徐建荣, 沈颂东, 张加梅, 等. 环境条件对中华绒螯蟹大眼幼体蜕壳生长的影响. 水产科学, 2006(10): 505-508 |
Xu LJ, Lü YH. China fishery statistical yearbook of 2018. Beijing: China Agriculture Press, 2018
|
徐乐俊, 吕永辉. 2018年中国渔业统计年鉴. 北京: 中国农业出版社, 2018
|
Yang JF, Zhu DF, Shen JM, et al. Physiological significance of crustacean hyperglycemic hormone family. Chinese Journal of Zoology, 2009, 44(1): 151-158 |
杨济芬, 朱冬发, 沈建明, 等. 甲壳动物高血糖激素家族生理功能研究进展. 动物学杂志, 2009, 44(1): 151-158 |
Yu ZJ, Zhang WB, Liu QG. Impact of culture pattern and light intensity on growth in pacific white leg shrimp and on water quality. Fisheries Science, 2016, 35(4): 321-326 |
俞震颉, 张文博, 刘其根. 不同养殖模式及光照对凡纳滨对虾生长和水质的影响. 水产科学, 2016, 35(4): 321-326 |
Yuan XC, Zhao WX. China fishery statistical yearbook of 2016. Beijing: China Agriculture Press, 2016
|
袁晓初, 赵文武. 2016年中国渔业统计年鉴. 北京: 中国农业出版社, 2016
|
Zhou XQ, Niu CJ, Li QF. Effects of light on feeding behavior growth and survival of aquatic animals. Acta Hydrobiologica Sinica, 2000(2): 178-181 |
周显青, 牛翠娟, 李庆芬. 光照对水生动物摄食、生长和存活的影响. 水生生物学报, 2000(2): 178-181 |
Zhou ZH, Fu WQ, Zhang WH. The effect of lights on the growth of Penaeus japonicus in laboratorial rasing. Fujian Animal Husbandry and Veterinary, 1999(2): 6-7 |
周志华, 傅文庆, 张文焕. 光线对实验室桶养日本对虾生长影响的研究. 福建畜牧兽医, 1999(2): 6-7 |



