2. 中国水产科学研究院黄海水产研究所 青岛海洋科学与技术试点国家实验室海洋渔业科学与食物产出过程功能实验室 农业农村部海水养殖病害防治重点实验室 青岛市海水养殖流行病学与生物安保重点实验室 山东 青岛 266071;
3. 大连海洋大学水产与生命学院 辽宁 大连 116023;
4. 青岛农业大学海洋科学与工程学院 山东 青岛 266109;
5. 山东农业大学动物科技学院 山东 泰安 271000;
6. 亚太水产养殖中心网 泰国 曼谷 10900;
7. 江苏数丰水产种业有限公司 江苏 高邮 255654;
1. College of Fisheries and Life Science, Shanghai Ocean University, Shanghai 201306, China
2. Yellow Sea Fisheries Research Institute, Chinese Academy of Fishery Sciences; Laboratory for Marine Fisheries Science and Food Production Processes, Pilot National Laboratory for Marine Science and Technology (Qingdao); Key Laboratory of Maricultural Organism Disease Control, Ministry of Agriculture and Rural Affairs; Qingdao Key Laboratory of Mariculture Epidemiology and Biosecurity, Qingdao, Shandong 266071, China;
3. College of Fisheries and Life Science, Dalian Ocean University, Dalian, Liaoning 116023, China;
4. College of Marine Science and Engineering, Qingdao Agricultural University, Qingdao, Shandong 266109, China;
5. College of Animal Technology, Shandong Agricultural University, Taixan, Shandong 271000, China;
6. Network of Aquaculture Centres in Asia-Pacific, Bangkok 10900, Thailand;
7. Jiangsu Shufeng Aquatic Seed Industry Co., Ltd., Gaoyou, Jiangsu 255654, China;
1. Jiangsu Shufeng Aquatic Seed Industry Co., Ltd., Gaoyou, Jiangsu 255654, China
罗氏沼虾(Macrobrachium rosenbergii)是世界上个体最大的淡水虾类之一,主要分布在东南亚、南亚国家及澳大利亚北部的淡水及咸淡水水域内(陈国孝, 1981)。因罗氏沼虾生物学特性优良,其养殖效益明显,被世界上许多国家和地区作为主要淡水养殖品种进行养殖。自1976年被引入我国以来,罗氏沼虾养殖业发展迅速(李增崇, 1987)。目前,我国罗氏沼虾年育苗量在250亿尾左右,养殖面积约为30 000 hm2,2019年我国罗氏沼虾养殖总产量达139 609 t (农业农村部渔业渔政管理局等, 2020),从苗种、饲料、成虾、加工到国内外贸易总产值超过100亿元,形成一条巨大的产业链,我国已成为世界上罗氏沼虾养殖产量最大的国家。
然而,2010年开始,罗氏沼虾养殖业中出现了以性早熟和生长缓慢为主要特征的铁虾综合征(iron prawn syndrome, IPS)问题(孙华良, 2013)。所谓“铁虾”,又称“铁壳虾”,是养殖户对性成熟早、壳硬、长不大的罗氏沼虾的一种称呼。一般指罗氏沼虾长到4~6 cm时出现生长缓慢,6~7 cm时已经性成熟,雌虾抱卵,雄虾的第2步足很长(袁锐等, 2017)。与水生动物大规模死亡事件不同,罗氏沼虾患IPS后并不出现明显死亡情况,仍正常吃料,但饵料系数很高,这与引起大规模死亡事件所造成的损失不同(孙华良, 2013, 袁锐等, 2017)。
甲壳动物的生殖发育受到多种激素和神经递质的调控。位于眼柄的X器官-窦腺复合体(XO-SG)是甲壳动物最重要的神经内分泌器官之一,分泌包括性腺抑制激素(GIH)、蜕皮抑制激素(MIH)、甲壳动物高血糖激素(CHH)等多种激素及5-羟色胺、多巴胺等神经递质,可调节甲壳动物的性腺发育、蜕皮、糖代谢、渗透压调节等生理过程(Nagaraju, 2011, Keller, 1992, 宋霞等, 2000)。但对于甲壳动物尤其是罗氏沼虾性腺发育的分子调控机制仍有待探索。
本研究采用Illumina Hiseq-2500平台对患IPS罗氏沼虾(IPS虾)和正常罗氏沼虾眼柄进行转录组测序,建立IPS虾和正常罗氏沼虾眼柄的转录组文库,鉴定可能在罗氏沼虾性早熟中起重要作用的差异表达基因和途径,对了解罗氏沼虾IPS的成因和分子机制具有重要参考意义。
1 材料与方法 1.1 样品采集实验用罗氏沼虾样品采集自江苏省的某罗氏沼虾养殖场。IPS虾样品取自表现出IPS症状的养殖池的偏小并有性成熟表现的个体,共取4份虾(T1、T2、T3和T4)的眼柄组织放入95%乙醇中干冰运送到实验室,取样虾的生物学体长为4.8~5.5 cm; 正常罗氏沼虾样品取自放苗时间相近、饲养管理方式相当的未表现出IPS症状的养殖池,共取3份虾(C1、C2和C3)的眼柄组织放入95%乙醇中干冰运送到实验室,取样虾的生物学体长为6.5~7.0 cm。
1.2 转录组测序样品的核酸提取、文库构建和测序提取4份IPS虾和3份正常罗氏沼虾眼柄样品的RNA,使用1%琼脂糖凝胶检测RNA的完整性,用NanoPhotometer® spectrophotometer (IMPLEN, 美国)和Qubit® RNA Assay Kit in Qubit® 2.0 Flurometer (Life Technologies, 美国)检测RNA纯度和浓度,用安捷伦生物分析仪2100系统(Agilent Technologie, 美国)的RNA Nano 6000检测试剂盒进一步评估RNA完整性。检测合格后,每个样品取1.5 µg RNA用于文库构建和测序。RNA-Seq文库构建和测序由北京诺禾致源生物科技有限公司完成,测序平台为Illumina Hiseq 2500,采用PE250测序。
1.3 测序数据组装及功能注释为保证信息分析质量,去除原始序列中含有接头和低质量的序列后得到clean reads。采用Trinity (Grabherr et al, 2011)进行拼接,将拼接所得的单基因序列(unigene)与Nr (NCBI non-redundant protein sequences)、Nt (NCBI nucleotide sequences)、PFAM (protein family)、KOG (eukaryotic ortholog groups)、Swissprot (a manually annotated and reviewed protein sequence database)、GO (gene ontology)和KEGG (Kyoto encyclopedia of genes and genomes)七大数据库进行比对注释,从而得到较为全面的基因功能注释信息和通路富集信息。
1.4 差异表达分析使用RSEM (Li et al, 2011)软件的bowtie 2程序将每个样本的clean reads比对到Trinity拼接获得的转录组上。通过比对结果可得到每个基因的测序数目(read count),并对其进行FPKM转换,进而分析基因的表达水平。采用DEGseq (Anders et al, 2010)软件进行差异分析,先对7个样本的数据进行矫正,再分别对IPS虾的4个生物学重复和正常虾的3个生物学重复取平均值,按组进行分析,筛选阈值为padj < 0.05。进一步使用GOseq (Young et al, 2010)软件在GO数据库中对差异表达基因进行分类注释; 使用KOBAS (Mao et al, 2005)软件对差异表达基因参与的代谢通路进行注释。
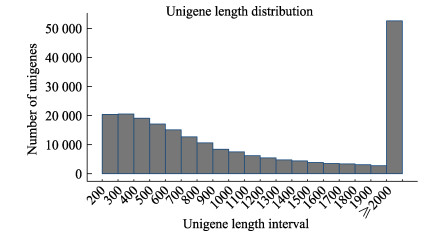
2 结果 2.1 转录组测序和序列组装通过RNA-Seq,本研究分别构建了患IPS罗氏沼虾和正常罗氏沼虾眼柄的cDNA文库,在3只正常虾和4只IPS虾眼柄中获得的raw reads及clean reads如表 1所示。用Trinity软件将获得的clean reads组装,共得到221 901条单基因序列,对应578 702个转录本,长度范围为201~30 985 bp(图 1),平均长度为1572 bp,N50长度为2867 bp,N90长度为646 bp。
|
|
表 1 转录组数据统计表 Tab.1 Statistics of transcriptome sequencing data |
|
图 1 单基因序列长度分布 Fig.1 Length distribution of assembled unigene |
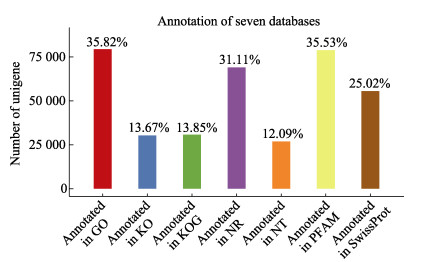
为获得全面的基因功能信息,使用Nr、Nt、Pfam、KOG、Swiss-prot、KEGG和GO数据库对得到的221 901条单基因序列进行基因功能注释,分别有69 094、26 846、78 844、30 744、55 540、30 354和79 503条单基因序列得到了注释。除此之外,有8594条单基因序列在7个数据库中都被注释,103 570条单基因序列在至少1个数据库中注释成功(图 2)。
|
图 2 单基因序列注释结果 Fig.2 Annotation results of unigene |
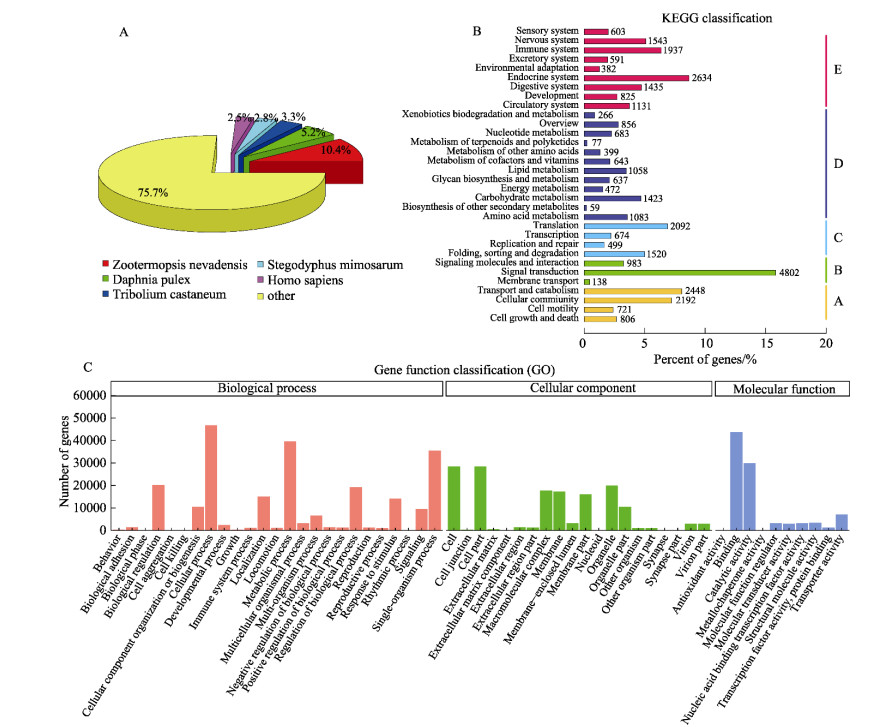
与Nr数据库比对结果显示,注释匹配的物种中,内华达古白蚁(Zootermopsis nevadensis)所占的比例最高,达到10.4%。其次是蚤状溞(Daphnia pulex)(5.2%)和赤拟谷盗(Tribolium castaneum)(3.3%)(图 3A)。KEGG分类注释结果显示,54 196条单基因序列可分为细胞过程、环境信息处理、遗传信息处理、代谢、有机系统5个分支中所含的32条二级通路,其中,运输和分解代谢(2448)、信号转导(4802)、翻译(2092)、碳水化合物代谢(1423)、内分泌系统(2634)是单基因序列二级通路数目最多的5个分支(图 3B)。GO数据库注释结果将注释成功的基因分为生物学过程、分子功能、细胞成分3个大类,有58 942条单基因序列注释到生物学过程中,64 920条单基因序列注释到分子功能中,46 242条单基因序列注释到细胞成分中。3个大类中注释单基因序列数目最多的功能分类为大分子代谢过程(28 058),核酸结合(13 469)和细胞内部分(25 489) (图 3C)。
|
图 3 转录组序列功能注释和分类 Fig.3 Functional annotation and classification of transcriptome sequences. A:NR数据库比对上的物种分布图; B:KEGG分类图; C:GO功能注释 A: Species distribution of Nr; B: KEGG classification map; C: Gene ontology (GO) assignment of assembled unigenes |
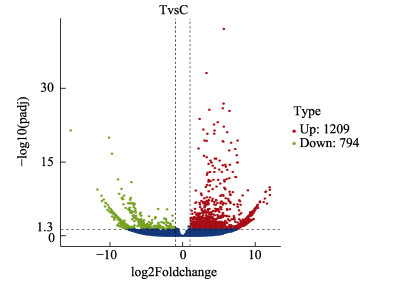
以padj < 0.05为阈值筛选在IPS虾和正常虾眼柄中差异表达的基因,结果见图 4。2003个基因在IPS虾和正常虾眼柄中差异表达,其中,1209个基因在IPS虾眼柄中上调,794个基因在IPS虾眼柄中下调。
|
图 4 基因差异表达分析火山图 Fig.4 Volcano plot of differentially expressed genes |
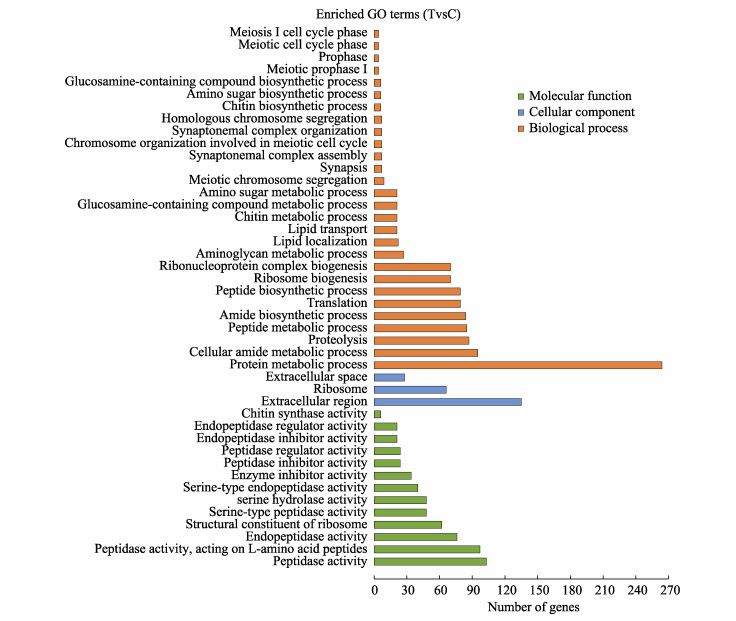
GO功能分类结果显示,808个差异基因被注释到3024条GO条目,44条显著富集,其中,生物学过程中显著富集28条,分子功能富集13条,细胞成份富集3条。蛋白质代谢过程在生物学过程中含有最多的单基因序列,肽酶活性在分子功能中含有最多的单基因序列,胞外区在细胞成分中含有最多的单基因序列(图 5)。
|
图 5 差异表达基因GO富集分析 Fig.5 GO assignment of differentially expressed genes |
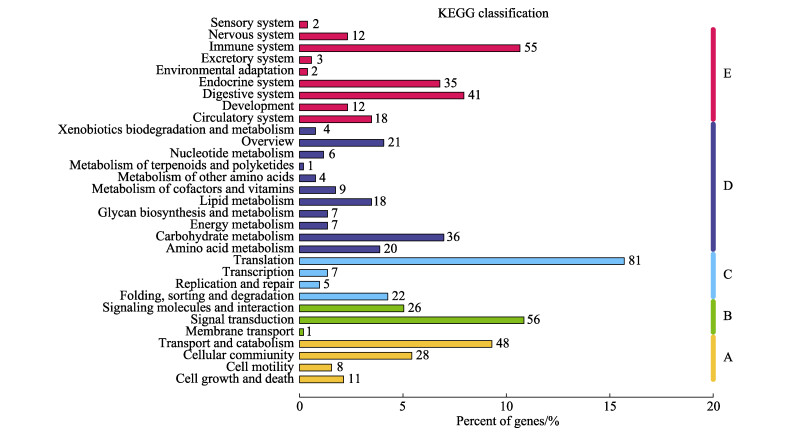
差异基因KEGG富集分析结果显示,516个差异基因被注释到242条KEGG通路,其中核糖体(ribosome)、金黄色葡萄球菌感染(Staphylococcus aureus infection)、脂肪消化吸收(fat digestion and absorption)、胰腺分泌物(pancreatic secretion)、矿物吸收(mineral absorption)、产生IgA的肠道免疫网络(intestinal immune network for IgA production) 6条通路显著富集。在KEGG 5大类通路中,翻译(81)、信号转导(56)和免疫系统(55)富集的差异基因数目最多(图 6)。
|
图 6 差异表达基因KEGG富集分析 Fig.6 KEGG assignment of differentially expressed genes |
根据KEGG功能富集分析结果及已发表文献,242条KEGG通路中与生殖调控相关的通路包括类固醇激素生物合成(steroid biosynthesis)、催乳素信号通路(prolactin signaling pathway)、雌激素信号通路(estrogen signaling pathway)、胰岛素信号通路(insulin signaling pathway)、促性腺激素释放激素信号通路(GnRH signaling pathway)、甲状腺激素信号通路(thyroid hormone signaling pathway)、胰高血糖素信号通路(glucagon signaling pathway)、催产素信号通路(oxytocin signaling pathway)、甲状腺激素合成(thyroid hormone synthesis)、谷氨酸能突触(glutamatergic synapse)、血清素能突触(serotonergic synapse)等。从这些通路中鉴定出C-4甾醇甲基氧化酶(C-4 sterol methyl oxidase)、UDP-葡萄糖4-差向异构酶(UDP-glucose 4-epimerase)、Ras相关GTPase (Ras-related GTPase)、胆碱转运体(choline transporter)、70 kDa热休克蛋白(heat shock 70 kDa protein)、雌激素相关受体蛋白(estrogen- related receptor protein)等基因下调表达,L-苏氨酸3-脱氢酶(L-threonine 3- dehydrogenase)、锌指蛋白(zinc finger protein)、雷帕霉素靶点(target of rapamycin)、NAD依赖性差向异构酶(NAD dependent epimerase)、90kDa热休克蛋白β (heat shock protein 90kDa beta)、谷氨酸脱羧酶(glutamate decarboxylase)、核受体共抑制因子1 (nuclear receptor corepressor 1)、芳香烃受体核转运体(aryl- hydrocarbon receptor nuclear translocator)等基因上调表达。
同时,发现溶酶体(lysosome)、抗原处理与呈递(antigen processing and presentation)、吞噬体(phagosome)、细胞凋亡(apoptosis)、过氧化物酶体(peroxisome)、B细胞受体信号通路(B cell receptor signaling pathway)、Toll样受体信号通路(toll-like receptor signaling pathway)等多条与免疫相关的通路(表 2)。从这些途径中筛选出血管内皮生长因子受体1、丝氨酸蛋白酶抑制剂6、C型凝集素2 (C-type lectin2)、芳基硫酸酯酶B、组织蛋白酶B (cathepsin B)、甲壳类抗菌肽4 (crustin 4)、锌指CCCH型抗病毒蛋白1样(zinc finger CCCH-type antiviral protein 1-like)、酚氧化酶原激活酶2a (prophenoloxidase-activating enzyme 2a)等多个在免疫反应中起重要作用的差异表达基因在IPS虾的眼柄中上调表达(表 3)。
|
|
表 2 与免疫相关的KEGG通路 Tab.2 KEGG pathways associated with immune |
|
|
表 3 显著上调的免疫相关差异表达基因 Tab.3 Immune-related DEGs up-regulated significantly |
为探索罗氏沼虾IPS的分子机制,本研究对患IPS罗氏沼虾和正常罗氏沼虾眼柄进行转录组测序。KEGG富集分析结果显示,在免疫系统中差异表达的基因的数量仅次于翻译和信号转导。根据已发表的文献和KEGG富集分析结果,鉴定出大量在机体免疫反应中起重要作用的通路和基因,提示可能存在病原微生物的感染。同时,KEGG和GO富集分析结果表明,正常虾和IPS虾眼柄中的各种激素和神经递质的合成和代谢存在差异。
1998年日本和越南报道了罗氏沼虾存在性早熟所致的生长缓慢(Hien et al, 1998)。在2008年印度就曾报道池塘养殖罗氏沼虾存在生长缓慢的问题,可能就是IPS的类似情况(Paulraj et al, 2008)。国内外多个团队对罗氏沼虾“铁虾”开展相关研究,Kutty等(2001)和Banu等(2015)通过一系列遗传学研究发现,体形较大的蓝爪雄虾或黄爪雄虾及体形较小的小雄虾3种雄虾的基因有明显的差异性; 周梦颖(2014)研究表明,温度、盐度和养殖密度可显著影响罗氏沼虾的生长及性腺发育。温度可影响罗氏沼虾眼柄中性腺抑制激素的表达(Qiao et al, 2015); 密度胁迫显著影响中国对虾(Penaeus chinensis)的生长及抗氧化能力(张海恩等, 2020)。周俊名等(2017)通过遗传多样性、水质、病原感染状况及白斑综合征病毒(WSSV)感染实验,探讨池养罗氏沼虾生长缓慢的原因,推测和水质、种质差异或退化等因素相比,感染特定病原引起罗氏沼虾生长缓慢的可能性更大。Gao等(2021)研究发现,一株阴沟肠杆菌(Enterobacter cloacae)与罗氏沼虾生长缓慢有关。本研究通过流行病学调查发现,正常虾苗在和IPS虾混养后会出现IPS症状,提示IPS具有传染性,推测IPS可能是由病原感染引起。
甲壳动物主要依靠先天免疫系统来抵御病原微生物的入侵,需要通过模式识别蛋白来识别病原,进而激发机体的免疫反应(Wang et al, 2013)。C型凝集素和凝集素是模式蛋白的一种,在本研究中,这2个基因在IPS虾眼柄中的表达量显著增加。之前的研究也呈现相似的结果,罗氏沼虾在感染罗氏沼虾野田村病毒(MrNV)、阴沟肠杆菌后,C型凝集素的表达量也显著上升(Pasookhush et al, 2019; Gao et al, 2020)。溶酶体和吞噬体是与免疫相关的KEGG通路中富集到差异表达基因数目最多的2条通路,组织蛋白酶B和组织蛋白酶L在这2条通路中起重要作用。组织蛋白酶是一种溶酶体内肽酶,可分解细胞和胞外蛋白质,在免疫反应中起重要作用(Turk et al, 2001)。越来越多的研究证明,组织蛋白酶L在甲壳动物免疫防御中起作用,如罗氏沼虾在感染MrNV、WSSV、嗜水气单胞菌(Aeromonas hydrophila)和哈维氏弧菌(Vibrio harveyi)后,组织蛋白酶L在血淋巴中的表达量显著增加(Arockiaraj et al, 2013b),中华绒螯蟹(Eriocheir sinensis)在感染鳗弧菌(V. anguillarum)后,组织蛋白酶L在血淋巴中的表达量也显著增加(Li et al, 2010)。甲壳类抗菌肽4是抗菌肽的一种,可阻止外来病原微生物的入侵,在海洋无脊椎动物先天免疫防御中起重要作用(Tincu et al, 2004)。罗氏沼虾在感染WSSV、传染性皮下和造血器官坏死病毒(IHHNV)及嗜水气单胞菌后,血淋巴中甲壳类抗菌肽的表达量增加(Arockiaraj et al, 2013a)。日本对虾(Penaeus japonicus)和斑节对虾(Penaeus monodon)在感染WSSV后也会出现类似结果(Hipolito et al, 2014, Antony et al, 2011),表明甲壳类抗菌肽对病毒入侵有一定的抵抗作用。
在虾类养殖业中通过单侧眼柄切除来促进亲虾的性腺发育(水燕等, 2013),切除眼柄后,GIH等激素分泌量下降进而促进亲虾性腺的发育。罗氏沼虾在性腺开始发育前,能量都集中在生长上,当性腺开始发育后,部分能量被用来支持性腺发育,进而影响生长。本研究的KEGG通路富集结果显示,类固醇激素、催乳素、雌激素、促性腺激素释放激素、胰岛素、血清素(5-羟色胺)等多种调控性腺发育激素的合成和代谢在IPS虾与正常虾间表现出差异,然而,在上述通路的27个差异表达基因中,仅有8个在IPS虾眼柄中的表达量增加。这可能是由于IPS虾的性腺发育已接近晚期,和正常虾相比,对这些激素的需求量减少,需要开展多个时间点的多组学分析,以明确上述表达在IPS虾中的作用和机制。
本研究对患IPS罗氏沼虾和正常罗氏沼虾的眼柄进行了转录组分析,除鉴定出与生殖调控相关的差异表达基因及途径外,还发现多个在甲壳动物先天免疫反应中起重要作用的基因在患IPS罗氏沼虾眼柄中的表达量上升,表明可能有病原体的感染。进一步的病原学研究表明,已知8种虾类致病病原均不是罗氏沼虾IPS致病病原,而一种新发现的传染性早熟病毒(infectious precocity virus, IPV)与IPS的发生密切相关(Dong et al, 2021),本研究支持这一研究结论。本研究为解析罗氏沼虾铁虾综合征的成因和分子机制奠定了基础。
ANDERS S, HUBER W. Differential expression analysis for sequence count data. Genome Biology, 2010, 11: R106 DOI:10.1186/gb-2010-11-10-r106 |
ANTONY S P, SINGH I S B, SUDHEER N S, et al. Molecular characterization of a crustin-like antimicrobial peptide in the giant tiger shrimp, Penaeus monodon, and its expression profile in response to various immunostimulants and challenge with WSSV. Immunobiology, 2011, 216(1/2): 184-194 |
AROCKIARAJ J, GNANAM A J, MUTHUKRISHNAN D, et al. Crustin, a WAP domain containing antimicrobial peptide from freshwater prawn Macrobrachium rosenbergii: Immune characterization. Fish and Shellfish Immunology, 2013a, 34(1): 109-118 DOI:10.1016/j.fsi.2012.10.009 |
AROCKIARAJ J, GNANAM A J, MUTHUKRISHNAN D, et al. Macrobrachium rosenbergii cathepsin L: Molecular characterization and gene expression in response to viral and bacterial infections. Microbiological Research, 2013b, 168(9): 569-579 DOI:10.1016/j.micres.2013.04.007 |
BANU M R, SIRAJ S S, CHRISTIANUS A, et al. Genetic variation among different morphotypes of the male freshwater prawn Macrobrachium rosenbergii. Aquaculture Reports, 2015, 1: 15-19 DOI:10.1016/j.aqrep.2015.02.001 |
Bureau of Fisheries and Fishery Administration under Ministry of Agriculture and Rural Affairs, Nation Fishery Technology Extension Center, China Society of Fisheries. China fishery statistical yearbook 2020. Beijing: China Agriculture Press, 2020: 158 [农业农村部渔业渔政管理局, 全国水产技术推广总站, 中国水产学会. 中国渔业统计年鉴. 北京: 中国农业出版社, 2020: 158]
|
CHEN G X. Macrobrachium rosenbergii. Chinese Journal of Zoology, 1981(3): 35-37 [陈国孝. 罗氏沼虾. 动物学杂志, 1981(3): 35-37] |
DONG X, WANG G H, HU T, et al. A novel virus of Flaviviridae associated with sexual precocity in Macrobrachium rosenbergii. mSystems, 2021, 6(3): e00003-21 DOI:10.1128/mSystems.00003-21 |
GAO X J, JIANG Z Y, ZHANG S M, et al. Transcriptome analysis and immune-related genes expression reveals the immune responses of Macrobrachium rosenbergii infected by Enterobacter cloacae. Fish and Shellfish Immunology, 2020, 101: 66-77 DOI:10.1016/j.fsi.2020.03.042 |
GAO X J, ZHOU Y F, ZHU X H, et al. Enterobacter cloacae: A probable etiological agent associated with slow growth in the giant freshwater prawn Macrobrachium rosenbergii. Aquaculture, 2021, 530: 735826 DOI:10.1016/j.aquaculture.2020.735826 |
GRABHERR M G, HAAS B J, YASSOUR M, et al. Full-length transcriptome assembly from RNA-Seq data without a reference genome. Nature Biotechnology, 2011, 29: 644-652 DOI:10.1038/nbt.1883 |
HIEN T T T, MINH T H, PHUONG N T, et al. Current status of freshwater prawn culture in the Mekong River Delta of Vietnam. JIRCAS Journal, 1998, 6: 89-100 |
HIPOLITO S G, SHITARA A, KONDO H, et al. Role of Marsupenaeus japonicus crustin-like peptide against Vibrio penaeicida and white spot syndrome virus infection. Developmental and Comparative Immunology, 2014, 46(2): 461-469 DOI:10.1016/j.dci.2014.06.001 |
KELLER R. Crustacean neuropeptides: Structures, functions and comparative aspects. Experientia, 1992, 48(5): 439-448 DOI:10.1007/BF01928162 |
KUTTY R, KURUP B M. Primary intrinsic factors governing the heterogenous individual growth in male morphotypes of Macrobrachium rosenbergii. International Conference on Fisheries, 2001, 165-173 |
LI B, DEWEY C N. RSEM: Accurate transcript quantification from RNA-Seq data with or without a reference genome. BMC Bioinformatics, 2011, 12(1): 323 DOI:10.1186/1471-2105-12-323 |
LI W W, JIN X K, HE L, et al. Molecular cloning, characterization, expression and activity analysis of cathepsin L in Chinese mitten crab, Eriocheir sinensis. Fish and Shellfish Immunology, 2010, 29(6): 1010-1018 DOI:10.1016/j.fsi.2010.08.007 |
LI Z C. Biology and artificial culture of Macrobrachium rosenbergii. Chinese Journal of Zoology, 1987, 22(2): 5-8 [李增崇. 罗氏沼虾生物学及人工养殖. 动物学杂志, 1987, 22(2): 5-8] |
MAO X Z, CAI T, OLYARCHUK J G, et al. Automated genome annotation and pathway identification using the KEGG Orthology (KO) as a controlled vocabulary. Bioinformatics, 2005, 21(19): 3787-3793 DOI:10.1093/bioinformatics/bti430 |
NAGARAJU G P. Reproductive regulators in decapod crustaceans: An overview. Journal of Experimental Biology, 2011, 214(1): 3-16 DOI:10.1242/jeb.047183 |
PASOOKHUSH P, HINDMARCH C, SITHIGORNGUL P, et al. Transcriptomic analysis of Macrobrachium rosenbergii (giant fresh water prawn) post-larvae in response to M. rosenbergii nodavirus (MrNV) infection: De novo assembly and functional annotation. BMC Genomics, 2019, 20(1): 762 DOI:10.1186/s12864-019-6102-6 |
PAULRAJ A, PEIXOTO S, VASUMATHI C, et al. Ovarian histology of stunted pond-reared Macrobrachium rosenbergii females. Aquaculture Research, 2008, 39(1): 64-69 |
QIAO H, XIONG Y W, ZHANG W Y, et al. Characterization, expression, and function analysis of gonad-inhibiting hormone in Oriental River prawn, Macrobrachium nipponense and its induced expression by temperature. Comparative Biochemistry and Physiology Part A: Molecular and Integrative Physiology, 2015, 185: 1-8 DOI:10.1016/j.cbpa.2015.03.005 |
SHUI Y, SHI Y H, XU Z H, et al. Advances of growth and development in crustaceans induced by eyestalk ablation. Guangdong Agricultural Sciences, 2013, 40(21): 124-126, 135 [水燕, 史永红, 徐增洪, 等. 眼柄切除快速诱导甲壳动物生长发育研究进展. 广东农业科学, 2013, 40(21): 124-126, 135 DOI:10.3969/j.issn.1004-874X.2013.21.033] |
SONG X, ZHOU K Y. Development of neurohormones in the eyestalk of crustacea. Chinese Journal of Zoology, 2000, 35(4): 39-43 [宋霞, 周开亚. 甲壳类的眼柄神经激素. 动物学杂志, 2000, 35(4): 39-43 DOI:10.3969/j.issn.0250-3263.2000.04.013] |
SUN H L. Gaoyou Macrobrachium rosenbergii encounters iron shrimp. Fisheries Advance Magazine, 2013(7): 39-41 [孙华良. 高邮罗氏沼虾遭遇铁虾困局. 海洋与渔业(水产前沿), 2013(7): 39-41] |
TINCU J A, TAYLOR S W. Antimicrobial peptides from marine invertebrates. Antimicrobial Agents and Chemotherapy, 2004, 48(10): 3645-3654 DOI:10.1128/AAC.48.10.3645-3654.2004 |
TURK V, TURK B, TURK D. Lysosomal cysteine proteases: facts and opportunities. The EMBO Journal, 2001, 20(17): 4629-4633 DOI:10.1093/emboj/20.17.4629 |
WANG X W, WANG J X. Pattern recognition receptors acting in innate immune system of shrimp against pathogen infections. Fish and Shellfish Immunology, 2013, 34(4): 981-989 DOI:10.1016/j.fsi.2012.08.008 |
YOUNG M D, WAKEFIELD M J, SMYTH G K, et al. Gene ontology analysis for RNA-seq: Accounting for selection bias. Genome Biology, 2010, 11(2): R14 DOI:10.1186/gb-2010-11-2-r14 |
YUAN R, ZHANG C H, CHEN H, et al. Phenomenon and research progress on prevention and control of "iron shell" in giant freshwater prawn. Fisheries Science, 2017, 36(3): 383-390 [袁锐, 张朝晖, 陈辉, 等. 罗氏沼虾"铁壳"现象及其防控研究进展. 水产科学, 2017, 36(3): 383-390] |
ZHANG H E, HE Y Y, LI J, et al. Effects of stocking density on growth, water quality, and antioxidant system of juvenile Fenneropenaeus chinensis. Progress in Fishery Sciences, 2020, 41(2): 140-149 [张海恩, 何玉英, 李健, 等. 密度胁迫对中国对虾幼虾生长、抗氧化系统功能及水质指标的影响. 渔业科学进展, 2020, 41(2): 140-149] |
ZHOU J M, DAI X L, JIANG F, et al. The preliminary analysis of the reasons for the poor growth of Macrobrachium rosenbergii in pond. Journal of Shanghai Ocean University, 2017, 26(6): 853-861 [周俊名, 戴习林, 蒋飞. 池养罗氏沼虾生长缓慢原因初步分析. 上海海洋大学学报, 2017, 26(6): 853-861] |
ZHOU M Y. Effect of stocking density, salinity and temperature on sex differentiation and early gonadal development on Macrobrachium rosenbergii. Masterxs Thesis of Shanghai Ocean University, 2014 [周梦颖. 养殖密度、盐度和温度对罗氏沼虾性别分化和早期性腺发育的影响. 上海海洋大学硕士研究生学位论文, 2014]
|




