2. 中国水产科学研究院黄海水产研究所 农业农村部海洋渔业可持续发展重点实验室 山东 青岛 266071;
3. 浙江海洋大学国家海洋设施养殖工程技术研究中心 浙江 舟山 316022;
4. 江苏海洋大学海洋科学与水产学院 江苏 连云港 222005;
5. 中国水产科学研究院长岛增殖实验站 山东 烟台 265800
2. Yellow Sea Fisheries Research Institute, Chinese Academy of Fishery Sciences, Key Laboratory of Sustainable Development of Marine Fisheries, Ministry of Agriculture and Rural Affairs, Qingdao, Shandong 266071, China;
3. National Engineering Research Center for Marine Aquaculture, Zhejiang Ocean University, Zhoushan, Zhejiang 316022, China;
4. College of Marine Science and Fisheries, Jiangsu Ocean University, Lianyungang, Jiangsu 222005, China;
5. Changdao Enhancement and Experiment Station, Chinese Academy of Fishery Sciences, Yantai, Shandong 265800, China
Foxl2是叉头状转录因子(forkhead transcription factor, Fox)超家族的成员之一,主要在垂体和卵巢中表达,通过转录调节其目的靶基因的转录、蛋白表达,参与生殖细胞的增殖与分化,在动物卵巢发育和维持中发挥重要作用(Uhlenhaut et al, 2011),与卵巢生殖细胞分化和卵巢功能的维持密切相关(Ellsworth et al, 2006; Boulanger et al, 2014)。
迄今为止,Foxl2基因功能的深入研究集中在脊椎动物和部分无脊椎动物,且结构高度保守。Foxl2是脊椎动物卵巢分化的特异性标志物(Alam et al, 2008)。据报道,Foxl2在蛙(Rana rugosa)卵巢分化的早期起关键作用(Oshima et al, 2008);是山羊(Capra hircus)雌性性别决定因子(Boulanger et al, 2014);Foxl2的失活会导致小鼠(Mus musculus)卵巢发育异常(Escalier et al, 2002);同时,敲除Foxl2和WNT4会导致小鼠表现出由雌性逆转为雄性的特征(Ottolenghi et al, 2008)。Foxl2在雄性鸡(Gus gallus)胚性腺中的错误表达抑制了睾丸发育途径(Major et al, 2019)。以上研究表明,Foxl2在脊椎动物卵巢中特异性表达,对卵巢的发育起着重要作用。相对于脊椎动物,Foxl2基因在无脊椎动物的研究较少。研究发现,Foxl2主要在栉孔扇贝(Chlamys farreri)和长牡蛎(Crassostrea gigas)的性腺和唇瓣中表达,其中,处于生长期卵巢的表达量是精巢的8倍(刘晓玲, 2012; Naimi et al, 2009)。在三角帆蚌(Hyriopsis cumingii)中,Foxl2主要表达于颗粒细胞中,与哺乳动物相似(叶容晖等, 2018)。
虾夷扇贝(Patinopecten yessoensis)因其多样的性别表现形式被认为是确定动物性别分化相关基因的最佳研究对象。虾夷扇贝隶属于瓣鳃纲(Lamellibranchia)、珍珠贝目(Pterioida)、扇贝科(Pectinidae),是我国北方重要的养殖经济物种。已有相关研究表明,Foxl2在扇贝雌性性腺中含量丰富(Li et al, 2018),可能是扇贝性别决定和分化的关键候选基因(Li et al, 2016)。但对于虾夷扇贝Foxl2基因在性腺发育中的时空表达模式尚未见有详细的报道。为进一步了解Foxl2在虾夷扇贝性腺发育不同时期中的表达特征,本研究克隆了虾夷扇贝Foxl2 cDNA编码区序列,进行生物信息学分析,并观察其组织表达规律,旨在为Foxl2在虾夷扇贝性腺发育过程中的功能提供科学依据。
1 材料与方法 1.1 实验材料实验用贝为2龄虾夷扇贝,购自山东烟台长岛生鲜市场,性腺生殖周期包含增长期、生长期、成熟期和排放期共4个时期,体重为(73.34±20.50) g。选取正常进食、排便的个体,取扇贝部分性腺组织用于RNA提取和组织分布检测,部分性腺组织浸入原位杂交固定液(Servicebio, 中国)中。组织切片法结合性腺组织涂片法鉴定性别。
1.2 总RNA提取和cDNA合成取大约50 mg冷冻的性腺组织,在研钵中用液氮充分研磨。采用Trizol法提取虾夷扇贝性腺总RNA,通过1.5%琼脂糖凝胶电泳检测RNA的完整性,NanoDrop 2000分光光度计(Thermo Scientific, 美国)检测其纯度与浓度,选取OD260 nm/280 nm值在1.90~2.2范围、RNA浓度>1000 ng/μL的样本进行反转录。RNA鉴定合格后,采用HiScriptⅢ RT SuperMix for qPCR (+gDNA wiper)试剂盒(Vazyme, 中国)并参照说明书合成cDNA。–20℃保存。
1.3 Foxl2基因的生物学分析虾夷扇贝转录组数据分析获得的基因编码序列与NCBI数据库比对,结果显示,与虾夷扇贝的Foxl2 (登录号:XM_021497746)完全吻合,命名为PyFoxl2。
采用ORF Finder (https://www.ncbi.nlm.nih.gov/orffinder/)确定PyFoxl2的开放阅读框。在线分析软件SMART(http://smart.embl-heidelberg.de/smart/set_mode.cgi?NORMAL=1)预测结构和功能域。使用SignalP 5.0 Server (http://www.cbs.dtu.dk/services/SignalP/)预测PyFoxl2蛋白的信号肽,并使用TMHMM 2.0 (http://www.cbs.dtu.dk/services/TMHMM/)预测跨膜区域。使用BLAST程序(https://blast.ncbi.nlm.nih.gov/Blast.cgi)对PyFoxl2进行碱基同源性分析,并进行蛋白质序列相似性搜索。使用swiss model (https://swissmodel.expasy.org/)预测蛋白三级结构。通过Jalview比对来自不同物种Foxl2的序列,并使用MEGA 7.0软件的Neighbor-Joining(NJ)方法构建PyFoxl2系统发育树。
1.4 半定量RT-PCR根据所获得的PyFoxl2 mRNA转录本序列,设计半定量RT-PCR引物Foxl2-F和Foxl2-R (表1)。以虾夷扇贝生长期的cDNA为模板,使用2×Taq Master Mix for PAGE试剂盒(Vazyme, 中国)对目的基因进行PCR扩增。反应条件:95℃ 3 min (预变性);95℃ 15 s,60℃ 15 s (退火),循环35次;72℃ 5 min (彻底延伸)。扩增产物经2.0%琼脂糖凝胶电泳检测目的基因。
1.5 荧光定量根据开放阅读框ORF (open reading frame)设计PyFoxl2定量qRT-PCR引物:QFoxl2-F和QFoxl2-R。使用β-actin基因(鲍相渤等, 2011)作为内参基因校正cDNA模板(表1)。
|
|
表 1 本实验所用引物 Tab.1 Primers used in this experiment |
分别以虾夷扇贝不同发育时期的性腺cDNA为模板对目的基因进行扩增。使用ChamQ SYBR Color qPCR master mix试剂盒(Vazyme, 中国)按照下列参数配制qPCR反应体系:2× ChamQ STBR Color qPCR master mix 10 μL,上下游引物各0.4 μL,cDNA模板2 μL,50× ROX reference dye 1 0.4 μL,灭菌蒸馏水6.8 μL。反应条件:95℃ 30 s(预变性);95℃ 10 s,60℃ 30 s (退火),循环40次;在StepOnePlusTM (美国)进行qPCR反应,每次反应3个重复,各个样品3个平行实验。本实验结果采取2–ΔΔCt法计算PyFoxl2基因的相对表达量。利用Prism 5软件对实验数据进行统计和分析。
1.6 原位杂交根据PyFoxl2基因的ORF区设计原位杂交探针YFoxl2。取部分性腺组织,切成2 mm左右的厚度,用灭菌的镊子置于原位杂交液中常温固定24 h用于切片处理。正式原位杂交步骤:固定的组织经石蜡切片后依次放入二甲苯Ⅰ 15 min–二甲苯Ⅱ 15 min–无水乙醇Ⅰ 5 min–无水乙醇Ⅱ 5 min–85%酒精5 min –75%酒精5 min–DEPC水洗。用胃蛋白酶处理,使靶核酸片段暴露,预杂交缓冲液(不含探针和硫酸葡聚糖)37℃孵育1 h,接着滴加含探针的杂交液,55℃杂交过夜。进行非特异结合探针的洗脱和残余RNA的消化后,用BSA(bovine serum albumin)封闭非特异性抗体1 h,滴加鼠抗地高辛标记488(anti-DIG-488)进行抗体孵育37℃ 40 min,洗涤,最后显色液(DAPI)进行显色,于尼康正置荧光显微镜(日本)下观察并采集图像。
2 结果 2.1 PyFoxl2序列分析生物信息学分析结果显示,PyFoxl2 ORF序列长度为1107 bp,编码368个氨基酸。存在保守的FH结构域(128~218 bp);FH结构域存在一个疑似核定位信号序列(nuclear localization signal sequence) RRRRMRR。PyFoxl2蛋白无信号肽,不存在明显的跨膜区域。因此,推测其为一个胞内蛋白,不属于膜蛋白。
2.2 PyFoxl2空间结构预测应用Swiss-Model同源建模服务器预测了PyFoxl2蛋白三维结构。结果显示,该蛋白保守区主要由3个α螺旋、4个β折叠和2个翼状结构组成(图1)。

|
图 1 PyFoxl2叉头保守区推测的三维结构 Fig.1 Schematic structure of PyFoxl2 forkhead domain |
从NCBI数据库里选择7个Foxl2代表性的物种的氨基酸序列进行同源比对分析。结果发现,PyFoxl2与软体动物的氨基酸序列相似度较高,其中,与栉孔扇贝、欧洲大扇贝(Pecten maximus)的相似性最高,分别为98%、96%,与美洲牡蛎(Crassostrea virginica)的相似性为73% (图2)。

|
图 2 虾夷扇贝Foxl2与其他物种的同源性序列比对 Fig.2 Foxl2 homologous sequence alignment between yesso scallop and other species 横线为FH结构域,红色的框为核定位信号序列物种NCBI登录号。栉孔扇贝:AFB35647.1;合浦珠母贝:QBX88970.1;美洲牡蛎:XP_022345405.1;欧洲大扇贝:XP_033724493.1;加州双斑蛸:XP_014785648.1;虾夷扇贝:XP_021353421.1;皱纹盘鲍:AWV50516.1。横线为DM结构域,红色的框为核定位信号序列 Species NCBI Login No. C. farreri: AFB35647.1; P. fucata: QBX88970.1; C. virginica: XP_022345405.1; P. maximus: XP_033724493.1; O. bimaculoides: XP_014785648.1; P. yessoensis: XP_021353421.1; H. discus hannai: AWV50516.1 The horizontal line is the forkhead domain, and the red box is the nuclear localization signal sequence |
为了了解Foxl2在不同物种中的进化关系,使用MEGA 7.0软件的Neighbor-Joining法对18个物种构建系统进化树。结果显示,软体动物聚为一支,无脊椎动物软体动物聚为一支,节肢动物门单独分出一支。其中,虾夷扇贝先与栉孔扇贝、长牡蛎、合浦珠母贝(Streptodera trachelostropha)等聚为一支,这显示它们的亲缘关系较近,形成的独立分支再与三角帆蚌聚为一支,最后与脉红螺(Rapana venosa)聚为一支,为软体动物门(Mollusca)(图3)。

|
图 3 不同物种Foxl2蛋白系统进化分析 Fig.3 Phylogenetic analysis of Foxl2 protein from different species |
RT-PCR分析PyFoxl2在虾夷扇贝生长期不同组织中的表达。结果显示,在鳃、肾、肝胰腺中都可检测到少量PyFoxl2转录本的存在,但在外套膜、闭壳肌中未见表达。PyFoxl2在卵巢中的表达量最高,其表达量显著高于精巢(图4)。

|
图 4 PyFoxl2在不同组织中的表达 Fig.4 The expression of PyFoxl2 in different tissues 1:DL 2000 marker;2:去离子水;3:鳃;4:外套膜;5:肾;6:肝胰腺;7:闭壳肌;8:卵巢;9:精巢 1: DL 2000 marker; 2: Deionized water; 3: Gill; 4: Mantle; 5: Kidney; 6: Hepatopancreas; 7: Adductor muscle; 8: Ovary; 9: Testis |
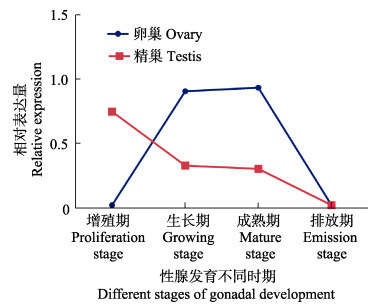
通过qRT-PCR分析构建了PyFoxl2在虾夷扇贝性腺发育的时空表达模型。结果显示,PyFoxl2在精巢的性腺发育周期中呈下降趋势;在卵巢中呈先上升后下降的趋势,其中,在成熟期达到最大值 (图5)。
|
图 5 PyFoxl2在虾夷扇贝性腺发育的时空表达模式 Fig.5 The expression pattern of PyFoxl2 in gonadal development of P. yessoensis |
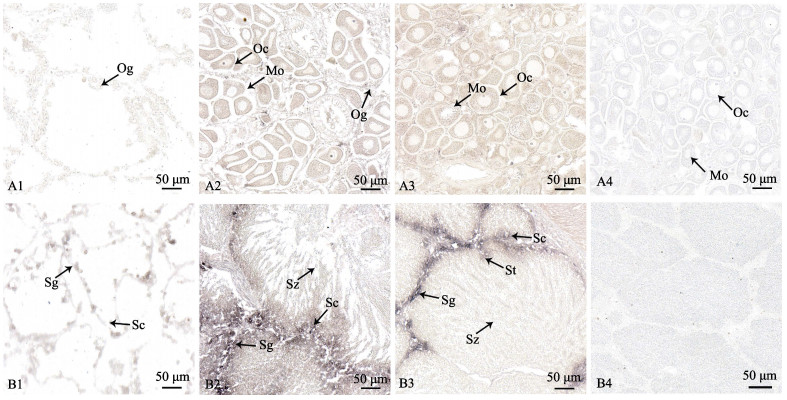
原位杂交结果显示,PyFoxl2定位于所有生殖细胞的细胞质。在卵巢中,与阴性对照组相比,PyFoxl2 mRNA在各时期的性腺分化细胞中均检测到阳性信号。其中,卵原细胞的阳性信号最弱(图6A1~A2)。PyFoxl2卵巢增殖期的阳性信号弱于生长期和成熟期。在精巢中,与阴性对照组相比,PyFoxl2在精原和精母细胞中的表达呈阳性。在成熟期精巢中,阳性信号随着生殖细胞的分化而逐渐减弱,精子中没有检测到信号(图6B1~B4)。
|
图 6 PyFoxl2在虾夷扇贝性腺发育不同时期的细胞学定位 Fig.6 Cytological localization of PyFoxl2 at different stages of gonadal development in P. yessoensis A:卵巢;B:精巢;1:增殖期;2:生长期;3:成熟期;4:阴性对照Mo:成熟卵;Oc:卵母细胞;Og:卵原细胞;Sc:精母细胞;Sg:精原细胞;St:精细胞;Sz:精子 A: Ovary; B: Testis; 1: Proliferation stage; 2: Growing stage; 3: Mature stage; 4: Negative control; Mo: Mature eggs; Oc: Oocyte; Og: Oogonium; Sc: Spermatocyte; Sg: Spermatogonium; St: Sperm cells; Sz: Sperm |
本研究分析了PyFoxl2的序列,发现其含有Fox基因家族的FH保守结构域序列特征。Fox家族都含有一个叉头样DNA结合区域,该叉头结构由90个氨基酸组成(曲中玉等, 2006),包含3个α螺旋、4个β折叠和2个翼状结构。其α螺旋与靶基因DNA双螺旋大沟结合,其β折叠则与小沟结合(Fan et al, 2011),以调控靶基因的表达。Foxl2是一个转录因子,该蛋白只有通过核膜进入细胞核内后,才能发挥其调控作用,而核定位信号序列是核内功能蛋白进入细胞核的结构基础,是一些蛋白进入细胞核内的必要片段。通过序列对比发现,在虾夷扇贝中发现的疑似核定位信号为RRRRRMRR,不同物种Foxl2的叉头框保守区都存在这个核定位信号序列。人(Homo sapiens) Foxl2蛋白也在保守区的C端具有一段精氨酸和赖氨酸区(RRRRRMKR),即Foxl2蛋白的细胞核定位信号序列,参与该蛋白由细胞质进入细胞核的调控(Beysen et al, 2008),该区域序列的突变将导致Foxl2转录因子不能顺利地进行亚细胞定位,只能聚集在细胞核外,影响其功能的正常发挥。虾夷扇贝Foxl2转录因子的疑似核定位信号如何引导其进入细胞核内并发挥功能有待今后进一步探讨。
对于不同物种的比较表明,Foxl2主要在卵巢中表达。除此之外,有学者在硬骨鱼类的脑垂体和鳃中检测到少量的表达,并认为Foxl2在脑–垂体–性腺轴中具有潜在的作用(Alam et al, 2008; Wang et al, 2004)。本研究通过RT-PCR在虾夷扇贝鳃、肾和肝胰腺中都检测到PyFoxl2转录本的存在。也有学者在三角帆蚌的研究中发现,Foxl2在性腺、鳃、闭壳肌、足部、外套膜和肾脏中均有表达,在卵巢的表达水平显著高于精巢(Wang et al, 2020)。在栉孔扇贝的肝胰腺有微弱的表达(刘晓玲, 2012)。以上研究提示,Foxl2基因功能不仅限于性腺和脑垂体方面,可能在其他组织中也具有一定的功能。
Loffler等(2003)研究认为,小鼠在性别决定后,Foxl2的表达立即上调,促进卵巢分化。本研究通过对虾夷扇贝性腺发育不同时期的时空表达分析发现,PyFoxl2在卵巢增殖期到生长期的表达量显著增加,维持在成熟期,而处于增殖期的虾夷扇贝性腺几乎可以判断出性别(高悦勉等, 2007)。因此,推断PyFoxl2可能也是在虾夷扇贝性别决定后表达上调。在精巢中,其表达量整体呈下降趋势。这个研究结果与长牡蛎中的相一致,在长牡蛎性腺中,生长期卵巢的表达量是精巢的8倍(Naimi et al, 2009)。长牡蛎性腺是一个季节性发育的非持续表达的器官,配子每年从生殖细胞开始增殖、分化、成熟。随着性腺小管的生长和分支,它们通过周围的结缔组织扩散,然后,结缔组织退化(Berthelin et al, 2001; Fabioux et al, 2004)。Foxl2在虾夷扇贝卵巢中的表达量随着性腺的发育呈先上升后下降的趋势,这个结果进一步证明Foxl2基因的表达与卵细胞分化息息相关。而原位杂交阳性信号变化验证了Foxl2在卵巢发育中的周期性表达变化。此外,通过原位杂交定位技术发现,PyFoxl2仅定位在虾夷扇贝的生殖细胞中,在成熟卵和卵母细胞中均检测到强阳性信号;随着雄性生殖细胞的逐级分化,阳性信号减弱。这个结果也与长牡蛎的一致,Naimi等(2009)认为这一结果可能提示Foxl2基因在长牡蛎精巢发育成熟过程中也有一定的作用。而在栉孔扇贝中,Foxl2不仅定位在生殖细胞中,在体细胞中也有阳性信号(刘晓玲, 2012)。由此推测,Foxl2对虾夷扇贝卵巢发育的调控起更重要的作用。
ALAM M A, KOBAYASHI Y, HORIGUCHI R, et al. Molecular cloning and quantitative expression of sexually dimorphic markers Dmrt1 and Foxl2 during female-to-male sex change in Epinephelus merra. General and Comparative Endocrinology, 2008, 157(1): 75-85 DOI:10.1016/j.ygcen.2008.03.018 |
BAO X B, LIU W D, JIANG B, et al. Expression stability of reference genes for quantitative PCR in Japanese scallop Patinopecten yessoensis. Fisheries Science, 2011, 30(10): 603-608 [内参基因在虾夷扇贝定量PCR中表达稳定性的比较. 水产科学, 2011, 30(10): 603-608 DOI:10.3969/j.issn.1003-1111.2011.10.003] |
BERTHELIN C H, LAISNEY J, ESPINOSA J, et al. Storage and reproductive strategy in Crassostrea gigas from two different growing areas (Normandy and the Atlantic coast, France). Invertebrate Reproduction and Development, 2001, 40(1): 79-86 DOI:10.1080/07924259.2001.9652500 |
BEYSEN D, MOUMN L, VEITIA R, et al. Missense mutations in the forkhead domain of Foxl2 lead to subcellular mislocalization, protein aggregation and impaired transactivation. Human Molecular Genetics, 2008, 17(13): 2030-2038 DOI:10.1093/hmg/ddn100 |
BOULANGER L, PANNETIER M, GALL L, et al. Foxl2 is a sex determining gene in the goat. Current Biology, 2014, 24(4): 404-408 DOI:10.1016/j.cub.2013.12.039 |
ELLSWORTH BS, EGASHIRA N, HALLER J L. Foxl2 in the pituitary: Molecular, genetic, and developmental analysis. Molecular Endocrinology, 2006, 20(11): 2796-2805 DOI:10.1210/me.2005-0303 |
ESCALIER D, ELOY L, GARCHON H J. Sex specific gene expression during meiotic prophase I: Xlr (X linked, lymphocyte regulated), not its male homologue Xmr (Xlr-related, meiosis regulated), is expressed in mouse oocytes. Biology of Reproduction, 2002, 67: 1646-1652 DOI:10.1095/biolreprod.102.006973 |
FABIOUX C, POUVREAU S, LE ROUX F, et al. The oyster vasa-like gene: A specific marker of the germline in Crassostrea gigas. Biochemical and Biophysical Research Communications, 2004, 315(4): 897-904 DOI:10.1016/j.bbrc.2004.01.145 |
FAN J Y, HAN B, QIAO J, et al. Functional study on a novel missense mutation of the transcription factor Foxl2 causes blepharophimosis-ptosis-epicanthus inversus syndrome (BPES). Mutagenesis, 2011, 26(2): 283-289 DOI:10.1093/mutage/geq086 |
GAO Y M, TIAN B, YU Y G, et al. The gonadal development and reproductive cycle of Japanese scallop Patinopecten yessoensis in Tahe Bay in Dalian. Journal of Dalian Fisheries University, 2007, 22(5): 335-339 [大连塔河湾海区虾夷扇贝的性腺发育与繁殖规律. 大连水产学院学报, 2007, 22(5): 335-339 DOI:10.3969/j.issn.1000-9957.2007.05.004] |
LI R J, ZHANG L L, LI W R, et al. Foxl2 and Dmrt1L are Yin and Yang genes for determining timing of sex differentiation in the bivalve mollusk Patinopecten yessoensis. Frontiers in Physiology, 2018, 9: 01166 DOI:10.3389/fphys.2018.01166 |
LI Y P, ZHANG L L, SUN Y, et al. Transcriptome sequencing and comparative analysis of ovary and testis identifies potential key sex-related genes and pathways in scallop Patinopecten yessoensis. Marine Biotechnology, 2016, 18: 453-465 DOI:10.1007/s10126-016-9706-8 |
LIU X L. Molecular cloning, expression pattern and function analysis of Cf-foxl2 in the scallop Chlamys farreri. Doctoral Dissertation of Ocean University of China, 2012 [刘晓玲. 栉孔扇贝Cf-foxl2基因的克隆、表达模式及功能初探. 中国海洋大学博士研究生学位论文, 2012]
|
LOFFLER K L, ZARKOWER D, KOOPMAN P, et al. Etiology of ovarian failure in blepharophimosis ptosis epicanthus inversus syndrome: Foxl2 is a conserved, early-acting gene in vertebrate ovarian development. Endocrinology, 2003, 144(7): 3237-3243 DOI:10.1210/en.2002-0095 |
MAJOR A T, AYERS K, CHUE J, et al. Foxl2 antagonises the male developmental pathway in embryonic chicken gonads. Journal of Endocrinology, 2019, 243(3): 211-228 DOI:10.1530/JOE-19-0277 |
NAIMI A, MARTINEZ A S, SPECQ M L, et al. Molecular cloning and gene expression of Cg-Foxl2 during the development and the adult gametogenetic cycle in the oyster Crassostrea gigas. Comparative Biochemistry and Physiology Part B:Biochemistry and Molecular Biology, 2009, 154: 134-142 DOI:10.1016/j.cbpb.2009.05.011 |
OSHIMA Y, UNO Y, MATSUDA Y, et al. Molecular cloning and gene expression of Foxl2 in the frog Rana rugosa. General and Comparative Endocrinology, 2008, 159(2/3): 170-177 |
OTTOLENGHI C, PELOSI E, TRAN J, et al. Loss of Wnt4 and Foxl2 leads to female-to-male sex reversal extending to germ cells. Human Molecular Genetics, 2008, 16(23): 2795-2804 |
QU Z Y, CHEN Z J. Foxl2: A transcription factor related with infertility. Reproduction and Contraception, 2006, 26(1): 40-43 [Foxl2—不孕有关的转录因子. 生殖与避孕, 2006, 26(1): 40-43 DOI:10.3969/j.issn.0253-357X.2006.01.008] |
UHLENHAUT N H, TREIER M. Forkhead transcription factors in ovarian function. Reproduction, 2011, 142(4): 489-495 DOI:10.1530/REP-11-0092 |
WANG D S, KOBAYASHI T, ZHOU L Y, et al. Molecular cloning and gene expression of Foxl2 in the Nile tilapia, Oreochromis niloticus. Biochemical and Biophysical Research Communications, 2004, 320(1): 83-89 DOI:10.1016/j.bbrc.2004.05.133 |
WANG G L, DONG S S, GUO P F, et al. Identification of Foxl2 in freshwater mussel Hyriopsis cumingii and its involvement in sex differentiation. Gene, 2020, 754: 144853 DOI:10.1016/j.gene.2020.144853 |
YE R H, RE H B. Molecular cloning and gene expression of foxl2 and sox14 gene from Hyriopsis cumingii. Oceanologia et Limnologia Sinica, 2018, 49(1): 160-167 [三角帆蚌(Hyriopsis cumingii)叉头蛋白2 (foxl2)基因和性别决定框14 (sox14)基因克隆与表达分析. 海洋与湖沼, 2018, 49(1): 160-167] |




